(Noticias de Nanowerk) Durante décadas, los investigadores han buscado un mejor control sobre la distribución y la actividad de los fármacos terapéuticos para minimizar los efectos secundarios adversos y maximizar la eficacia. La mayoría de los medicamentos aprobados, como las moléculas pequeñas y los anticuerpos monoclonales, funcionan sistémicamente con poca precisión innata sobre dónde se acumulan en el cuerpo y cuánto tiempo persisten. Esta falta de precisión desencadena reacciones tóxicas y desalienta las dosis altas, lo que limita el progreso. Recientemente, los avances en materia estructural nanotecnología de ADN han abierto un camino completamente nuevo para ejercer una gobernanza espacial sobre el comportamiento de las drogas utilizando nanoestructuras programables y autoensamblables con formas y química definidas. A diferencia de los portadores de fármacos pasivos anteriores, como los liposomas y los polimerosomas, estos sistemas inteligentes de ADN presentan programabilidad modular, geometría precisa a nanoescala y fracciones de superficie fácilmente sintonizables que confieren direccionalidad. En un nuevo estudio publicado en Informes científicos (“Biodistribución y función de nanoestructuras de origami de ADN-polímero acoplado”), los investigadores demuestran el poder de acoplar aptámeros dirigidos a enfermedades a nanoestructuras de ADN estabilizadas con polietilenglicol (PEG) para concentrar y mantener la actividad terapéutica dentro de los sitios del tejido objetivo. Los investigadores exploraron múltiples nanoestructuras en forma de varilla con diferentes tamaños y relaciones de aspecto, descubriendo que las partículas más largas por encima de 100 nm persistían mucho más tiempo. in vivo mientras se difunde más lentamente fuera de los lugares de inyección.
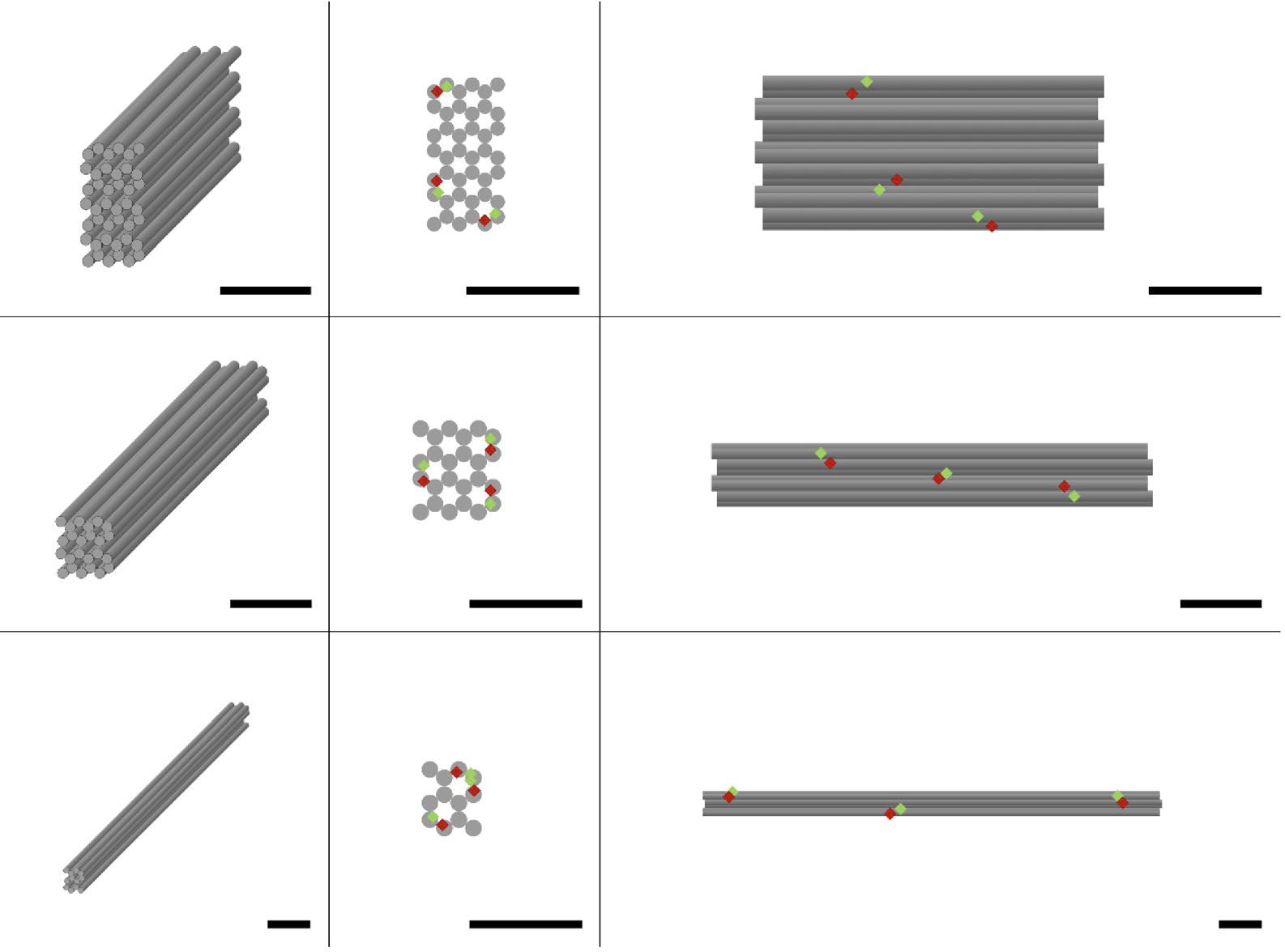 Caracterización estructural de las nanoestructuras de origami de ADN y evaluación de la calidad de su ensamblaje. (a) Esquema de diseño. Las filas muestran las diferentes nanoestructuras de origami de ADN investigadas: cuboide, varilla corta y varilla larga (de arriba a abajo). Las columnas muestran diferentes vistas de las nanoestructuras de origami de ADN: 3D, vista frontal y lateral (de izquierda a derecha). Los pares FRET se distribuyen uniformemente en las nanoestructuras de origami de ADN y se muestran como diamantes rojos y verdes. Todas las barras de escala son de 20 nm. (© NPG) La unión de aptámeros dirigidos contra la citoquina inflamatoria TNF-alfa confirió efectos antiinflamatorios en modelos murinos de reacciones de hipersensibilidad de tipo retardado (DTHR). Los ratones tratados con nanoestructuras de ADN que neutralizan el TNF-alfa mostraron una reducción de la inflamación del tejido, una menor infiltración de células inmunes y un menor engrosamiento epidérmico comparable a los anticuerpos monoclonales anti-TNF-alfa. Sin embargo, a diferencia de los anticuerpos convencionales dispersos sistémicamente por todo el cuerpo, las nanoestructuras de aptámero permanecieron concentradas en el tejido objetivo. Este efecto de localización centra el impacto terapéutico en los sitios de la enfermedad evitando al mismo tiempo la exposición sistémica, aumentando así la ventana terapéutica. También reduce la dosis necesaria para obtener resultados de tratamiento equivalentes. La modularidad de estas nanoestructuras programables permite aún más la optimización y multiplexación personalizadas mediante la fácil sustitución de fracciones terapéuticas y de direccionamiento. Los hallazgos resaltan el potencial disruptivo de las nanoestructuras de ADN autoensambladas como portadores inteligentes de fármacos con control espacial inherente. A medida que los costos continúan cayendo exponencialmente, estos sistemas de ADN de precisión podrían reemplazar tecnologías convencionales como los anticuerpos monoclonales para mejorar la especificidad y, al mismo tiempo, acelerar el desarrollo de cócteles de aptámeros sinérgicos, la administración de fármacos localizada en tejidos y la medicina personalizada adaptada a la genética individual y los fenotipos de enfermedades.
Caracterización estructural de las nanoestructuras de origami de ADN y evaluación de la calidad de su ensamblaje. (a) Esquema de diseño. Las filas muestran las diferentes nanoestructuras de origami de ADN investigadas: cuboide, varilla corta y varilla larga (de arriba a abajo). Las columnas muestran diferentes vistas de las nanoestructuras de origami de ADN: 3D, vista frontal y lateral (de izquierda a derecha). Los pares FRET se distribuyen uniformemente en las nanoestructuras de origami de ADN y se muestran como diamantes rojos y verdes. Todas las barras de escala son de 20 nm. (© NPG) La unión de aptámeros dirigidos contra la citoquina inflamatoria TNF-alfa confirió efectos antiinflamatorios en modelos murinos de reacciones de hipersensibilidad de tipo retardado (DTHR). Los ratones tratados con nanoestructuras de ADN que neutralizan el TNF-alfa mostraron una reducción de la inflamación del tejido, una menor infiltración de células inmunes y un menor engrosamiento epidérmico comparable a los anticuerpos monoclonales anti-TNF-alfa. Sin embargo, a diferencia de los anticuerpos convencionales dispersos sistémicamente por todo el cuerpo, las nanoestructuras de aptámero permanecieron concentradas en el tejido objetivo. Este efecto de localización centra el impacto terapéutico en los sitios de la enfermedad evitando al mismo tiempo la exposición sistémica, aumentando así la ventana terapéutica. También reduce la dosis necesaria para obtener resultados de tratamiento equivalentes. La modularidad de estas nanoestructuras programables permite aún más la optimización y multiplexación personalizadas mediante la fácil sustitución de fracciones terapéuticas y de direccionamiento. Los hallazgos resaltan el potencial disruptivo de las nanoestructuras de ADN autoensambladas como portadores inteligentes de fármacos con control espacial inherente. A medida que los costos continúan cayendo exponencialmente, estos sistemas de ADN de precisión podrían reemplazar tecnologías convencionales como los anticuerpos monoclonales para mejorar la especificidad y, al mismo tiempo, acelerar el desarrollo de cócteles de aptámeros sinérgicos, la administración de fármacos localizada en tejidos y la medicina personalizada adaptada a la genética individual y los fenotipos de enfermedades.
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- PlatoData.Network Vertical Generativo Ai. Empodérate. Accede Aquí.
- PlatoAiStream. Inteligencia Web3. Conocimiento amplificado. Accede Aquí.
- PlatoESG. Carbón, tecnología limpia, Energía, Ambiente, Solar, Gestión de residuos. Accede Aquí.
- PlatoSalud. Inteligencia en Biotecnología y Ensayos Clínicos. Accede Aquí.
- Fuente: https://www.nanowerk.com/nanotechnology-news2/newsid=64109.php



