La lesión cerebral traumática (TBI), causada por una sacudida o impacto repentino en la cabeza, requiere un diagnóstico lo más rápido posible. Para evitar daños irreversibles, las decisiones de tratamiento críticas para la vida deben tomarse dentro de la “hora dorada” posterior al trauma. Sin embargo, diagnosticar una lesión cerebral traumática en el lugar de atención es difícil, ya que se basa en observaciones realizadas por equipos de ambulancia seguidas de investigaciones radiológicas como resonancias magnéticas o tomografías computarizadas al llegar al hospital.
Para permitir una intervención más oportuna, investigadores del Universidad de Birmingham están desarrollando un dispositivo de diagnóstico portátil que detecta TBI al apuntar un láser seguro al ojo. El dispositivo, descrito en Science Advances, está diseñado para usarse tan pronto como se produce una lesión, ya sea en la carretera, en el campo de batalla o en el campo deportivo, para evaluar a los pacientes en busca de TCE, determinar la gravedad del trauma y dirigir el tratamiento en consecuencia.
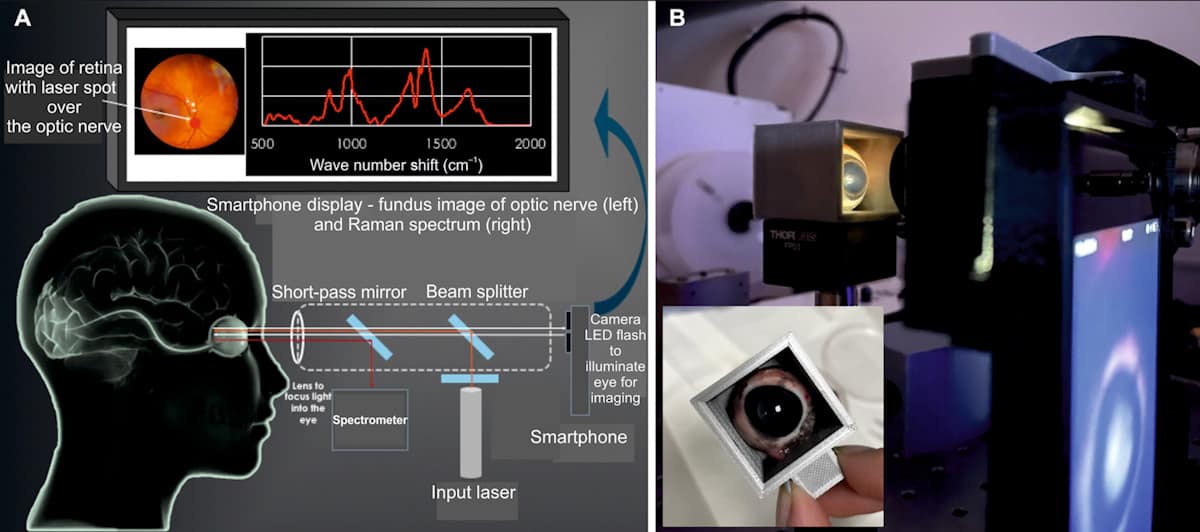
El dispositivo seguro para los ojos (EyeD) se basa en la espectroscopia Raman, una técnica óptica que utiliza la dispersión inelástica de luz láser para sondear la composición molecular. Funciona haciendo brillar un láser de clase 635 de 1 nm sobre la córnea. A continuación, la óptica del propio ojo enfoca el haz colimado sobre la retina. Para apuntar el láser a la región de interés, el sistema EyeD realiza simultáneamente imágenes del fondo de ojo y análisis espectroscópico utilizando la cámara de un teléfono inteligente para visualizar la parte posterior del ojo.
Los espectros Raman recopilados de la retina y el nervio óptico se analizan para detectar la presencia de cambios bioquímicos específicos de TBI, utilizando el algoritmo de red neuronal artificial SKiNET como herramienta de apoyo a la toma de decisiones. Como la retina y el nervio óptico están tan estrechamente vinculados al cerebro, los cambios en los biomarcadores después de una lesión reflejarán cambios bioquímicos en el microambiente cerebral.
“Nuestro dispositivo permitirá el diagnóstico temprano de TBI mediante la evaluación directa de los cambios agudos de angustia en tiempo real en el tejido nervioso neurorretiniano/óptico vivo. Nos permite examinar el tejido del sistema nervioso central de forma directa y no invasiva”, explica el líder del equipo. Pola Goldberg Oppenheimer. "El análisis de la neurorretina como una proyección del sistema nervioso central proporciona una ventana a la bioquímica del cerebro".
Estudios espectroscópicos
Para probar el rendimiento de su dispositivo de imágenes, Oppenheimer y sus colegas construyeron un fantasma de tejido que imita las dimensiones físicas y las características ópticas del ojo, al tiempo que proporciona una firma Raman realista de la retina. El fantasma incluye una lente, un orificio de 4 mm de diámetro que representa la pupila no dilatada y un soporte para muestras de tejido retiniano.
El equipo demostró que el dispositivo EyeD podía enfocar eficazmente el rayo láser en la posición deseada de la retina. Los espectros medidos desde el fantasma de tejido resolvieron las principales bandas Raman en la región de alto número de ondas, que se pueden utilizar para distinguir varios tipos de tejidos.
A continuación, los investigadores utilizaron el dispositivo prototipo para analizar muestras de retina de ojos de cerdo, que son similares a los ojos humanos en tamaño, estructura, desarrollo y composición. Recolectaron 510 mediciones de 39 muestras de retina con TBI y 12 muestras de control, registrando espectros cercanos al disco óptico. En general, los espectros Raman mostraron varias bandas características en el rango de 1200-1700 cm.-1 región de huellas dactilares, además de una mejora de las bandas de alto número de ondas en los 2800-3200 cm-1 región.

El uso de SKiNET para crear mapas de optimización automática (SOM) que muestran la agrupación de los espectros Raman retinianos reveló una clara separación entre las retinas con TBI y las muestras de control. Esto surge porque los espectros Raman reflejan variaciones bioquímicas en el ojo después de una lesión cerebral traumática. Por ejemplo, la TBI aumenta el contenido de lípidos y proteínas en el ojo, lo que hace que los picos que se originan en ellos se vuelvan más pronunciados en los espectros Raman.
Los cambios espectrales más significativos en respuesta al TBI se debieron a las contribuciones de los lípidos cerebrales cardiolipina y citocromo C, que se manifestaron como un aumento en la proporción entre los 2930 y los 2850 cm-XNUMX.-1 pico en el espectro Raman. Los investigadores utilizaron características seleccionadas de la relación de picos 2850/2930 y las intensidades de seis picos característicos de los espectros de TBI para formar la clasificación SKiNET, produciendo un código de barras espectroscópico para la detección de TBI.
Para evaluar la capacidad del sistema EyeD para diferenciar TBI a través de cambios retinianos, calcularon el área bajo la curva (AUC) para cada pico y la proporción de picos 2930/2850, y trazaron las tasas de verdaderos positivos frente a falsos negativos. El uso de la optimización SKiNET con validación cruzada de 10 veces en los datos de entrenamiento dio como resultado una precisión de clasificación del 90.7 ± 0.9 %. Este resultado indica que los cambios en la proporción máxima de 2930/2850 después de una TBI podrían proporcionar un indicador valioso para discriminar la TBI de los controles sanos.
"El uso simultáneo de espectroscopia Raman e imágenes del fondo de ojo, empaquetado como un dispositivo portátil de bajo costo, proporciona el primer camino tangible hacia el diagnóstico no invasivo de TBI en el lugar de atención", dice Oppenheimer. Mundo de la física.

Para las conmociones cerebrales, los ojos son ventanas al cerebro
El siguiente paso será optimizar el prototipo para su validación clínica. Para facilitar la traducción clínica, los investigadores planean reemplazar el espectrómetro independiente con un espectrómetro compacto en el dispositivo y una lectura de teléfono inteligente, lo que permitirá la fotografía del fondo de ojo y la espectroscopia Raman a través de una única pantalla de teléfono inteligente.
"Actualmente estamos diseñando un dispositivo desplegable fácil de usar, integrado con nuestro algoritmo de red neuronal artificial para la interpretación automatizada de los resultados sin necesidad de soporte especializado, clasificando rápidamente los datos espectrales", dice Oppenheimer. “[También estamos] evaluando clínicamente la usabilidad del dispositivo en voluntarios sanos y en pacientes para demostrar su potencial para el diagnóstico en tiempo real. Después de establecer la tolerabilidad y usabilidad del dispositivo, procederemos a realizar la primera evaluación en humanos y un ensayo clínico a pequeña escala”.
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- PlatoData.Network Vertical Generativo Ai. Empodérate. Accede Aquí.
- PlatoAiStream. Inteligencia Web3. Conocimiento amplificado. Accede Aquí.
- PlatoESG. Carbón, tecnología limpia, Energía, Ambiente, Solar, Gestión de residuos. Accede Aquí.
- PlatoSalud. Inteligencia en Biotecnología y Ensayos Clínicos. Accede Aquí.
- Fuente: https://physicsworld.com/a/handheld-device-uses-eye-safe-retinal-spectroscopy-to-diagnose-brain-injury/



