IA en el descubrimiento de fármacos de un vistazo
El aumento continuo de la inteligencia artificial (IA) está afectando significativamente a varias industrias, y los sectores farmacéutico y biotecnológico no son una excepción. No sorprende que tanto las organizaciones farmacéuticas grandes como las pequeñas estén adoptando cada vez más plataformas de descubrimiento de fármacos de IA para agilizar los procesos de investigación y desarrollo, reducir los tiempos y costos de descubrimiento y mejorar la eficiencia general.
Compañías farmacéuticas líderes como J&J, GSK, AstraZeneca, Novartis, Pfizer, Sanofi y Eli Lilly, entre otras, han realizado importantes inversiones en IA para el descubrimiento de fármacos. Estas inversiones incluyen inversiones de capital, adquisiciones o asociaciones con empresas centradas en IA, desarrollo de capacidades internas o una combinación de estas estrategias.
Al mismo tiempo, hay una oleada de empresas de biotecnología y descubrimiento de fármacos novedosos que se establecen como organizaciones centradas en la IA, a menudo desde su creación. Fundadas principalmente en la última década, estas empresas ya han construido y probado plataformas especializadas de descubrimiento de fármacos impulsadas por IA. Estas plataformas a menudo incorporan numerosos modelos de aprendizaje automático y ahora están comenzando a generar beneficios significativos en términos de capacidades de diseño de fármacos y descubrimiento de objetivos rápidos y rentables. Como resultado, están produciendo candidatos a fármacos preclínicos y clínicos a un ritmo acelerado. En las siguientes secciones, exploraremos una selección de candidatos a fármacos desarrollados por IA, incluidas moléculas pequeñas, productos biológicos y otras modalidades, que ya han ingresado a ensayos clínicos o están a punto de hacerlo.
Además, ciertas empresas de inteligencia artificial han logrado avances en el modelado de la biología utilizando datos multimodales complejos a escalas que eran inimaginables hace solo dos décadas. Otro grupo de empresas ha desarrollado plataformas impulsadas por IA para mejorar la eficiencia operativa y el diseño de experimentos en ensayos clínicos o análisis de datos del mundo real, como la farmacovigilancia.
Las principales corporaciones tecnológicas, como Alphabet, Microsoft, Amazon, IBM y Tencent, poseen experiencia en inteligencia artificial y tecnologías de big data, y también se están aventurando en el espacio del descubrimiento de fármacos. Su participación incluye invertir, fundar nuevas empresas, asociarse con empresas de ciencias de la vida, experimentar e innovar.
Por último, se han logrado avances significativos en otras tecnologías avanzadas, como la computación cuántica, Cryo-EM y bibliotecas codificadas por ADN. Estas tecnologías están convergiendo con la tendencia de la IA, lo que da como resultado no solo nuevos tipos de herramientas, productos y servicios, sino también una ola de nuevas empresas innovadoras e incluso modelos comerciales novedosos.
¿Qué es la IA y cómo se aplica en el descubrimiento de fármacos?
La inteligencia artificial es un concepto relativamente antiguo, formalizado en una famosa conferencia de Dartmouth College en 1956. Las tecnologías de IA en el descubrimiento de fármacos han evolucionado a partir de conceptos y enfoques anteriores de aprendizaje automático (ML), quimioinformática y bioinformática. Por ejemplo, la aplicación del aprendizaje automático para desarrollar modelos cuantitativos de relación estructura-actividad (QSAR) y sistemas expertos para la predicción de toxicidad tiene una larga historia.
Sin embargo, el rápido (en algunos casos, “exponencial”) advenimiento de big data, análisis avanzados, minimización del costo de computación, aceleración de GPU, computación en la nube, desarrollo de algoritmos (por ejemplo, redes neuronales profundas y modelos de lenguaje extenso) y la “democratización” de la tecnología de IA — todo condujo a un “boom” sinérgico en la comercialización e industrialización de la inteligencia artificial, en particular, en las industrias farmacéutica y biotecnológica.
En este documento técnico, usamos el término colectivo "inteligencia artificial" para referirnos a cualquier sistema computacional y de modelado sofisticado que pueda aprender automáticamente información y derivar sugerencias prácticas de "big data", datos estructurados y no estructurados, también datos multimodales.
Si bien no hay límite para una familia particular de algoritmos a los que nos referimos como "inteligencia artificial", en la mayoría de los casos, implicamos varios tipos de sistemas basados en aprendizaje automático (principalmente redes neuronales profundas) y gran procesamiento de lenguaje natural (NLP) modelos Los sistemas de IA modernos pueden aprender sin recibir instrucciones explícitas (en contraste con el software de quimioinformática tradicional dentro de la lógica "si-entonces"), pueden mejorar la precisión después de nuevos ciclos de aprendizaje y cuando se alimentan más datos al sistema y, lo más notable, pueden procesar datos multimodales de gran dimensionalidad y tamaño enorme. Todos estos atributos son los que diferencian significativamente los sistemas de inteligencia artificial modernos de los paquetes de software heredados de quimioinformática y bioinformática. Tales habilidades están en el centro de lo que impulsa el entusiasmo continuo por la IA (y la exageración).
Si bien casi todas las organizaciones farmacéuticas y laboratorios académicos utilizan algunos componentes de lo que llamamos "inteligencia artificial", por ejemplo, herramientas de aprendizaje automático y modelos de lenguaje, algunas empresas lograron construir sofisticados canales computacionales y de modelado, investigar "plataformas de IA". que incluyen flujos de trabajo automatizados en docenas e incluso cientos de diversos modelos y sistemas (aprendizaje profundo, modelos de lenguaje) y cientos de diversas fuentes de datos públicas y propietarias.
La alta sofisticación y automatización de algunas plataformas de IA condujo a su "commoditización" hasta el punto de que tienen nombres comerciales registrados. Al mismo tiempo, algunos de ellos se ofrecen como software como servicio a otras empresas. Los ejemplos incluyen mRNA DESIGN STUDIO™ de Moderna, Centaur Chemist® de Exscientia, Guardian Angel™ de AI Therapeutics, ConVERGE™ de Verge Genomics, Taxonomy3® de C4X Discovery y muchos otros.
A continuación se muestra un ejemplo de Pharma.AI de Insilico Medicine, un sistema modular para el descubrimiento de fármacos de extremo a extremo que comprende cientos de subsistemas y modelos de aprendizaje automático diferentes, controlados en su totalidad por otros algoritmos de abstracción de modelado superior (a través de un principio de “aprendizaje en conjunto”).
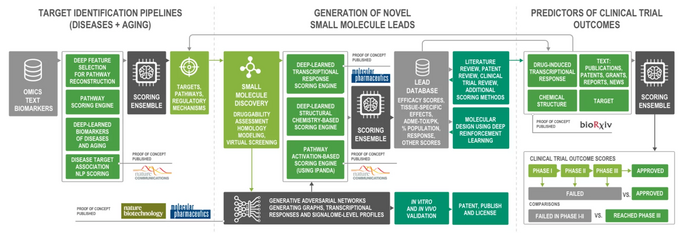
Un esquema de la plataforma de extremo a extremo de Pharma.AI. Credito de imagen: https://insilico.com
La inteligencia artificial se usa ampliamente en casi todos los aspectos de la investigación farmacéutica, desde la extracción de datos, el modelado biológico y el descubrimiento de objetivos hasta la identificación de plomo y la investigación clínica y preclínica. También se utiliza para la planificación de síntesis, la búsqueda inteligente de reactivos y consumibles de investigación y tareas auxiliares como cuadernos de laboratorio inteligentes y asistentes virtuales.

Fuente: https://www.biopharmatrend.com/m/companies/ai/
El ecosistema de Life Science de los adoptantes de IA incluye las siguientes categorías principales de jugadores:
|
Más de 400 empresas impulsadas por IA (startups/ampliaciones), que ofrecen una amplia gama de plataformas y servicios impulsados por IA, desde el modelo clásico de software como servicio hasta servicios de ciencia de datos personalizados, descubrimiento de fármacos ("candidato a fármaco como servicio") y soporte/gestión de ensayos clínicos recursos. |
|
Los proveedores de software de dominio específico (p. ej., KNIME, ChemAxon, Dotmatics, MolSoft y otros) se centran principalmente en el software de quimioinformática/bioinformática, pero también ofrecen herramientas basadas en el aprendizaje automático. |
|
Compañías farmacéuticas y biotecnológicas de primer nivel que desarrollan experiencia interna en IA como parte de su estrategia de I+D. Dichos jugadores a menudo colaboran con proveedores externos de IA y nuevas empresas de biotecnología impulsadas por IA para explorar programas piloto en descubrimiento de fármacos/biología básica/análisis de ensayos clínicos. |
|
Empresas de tecnología de primer nivel como Google, Amazon y Tencent ingresan al espacio farmacéutico, aprovechando las tecnologías de IA de vanguardia y las infraestructuras de big data. |
|
Organizaciones de investigación por contrato (CRO) que desarrollan experiencia en IA para aumentar su oferta de valor a los clientes farmacéuticos/biotecnológicos |
|
Laboratorios académicos en el espacio farmacéutico/biotecnológico, que realizan investigaciones de IA y desarrollan marcos y herramientas especializados relevantes para la industria (generalmente una cuna para futuras empresas emergentes/spin-outs de IA) |
|
Proveedores de software no específicos de dominio que desarrollan paquetes y modelos de IA como servicio adecuados para su aplicación en la investigación farmacéutica (por ejemplo, "IA lista para usar") |
|
Marcos y herramientas de aprendizaje automático de código abierto, ampliamente explotados por profesionales de las ciencias de la vida en sus proyectos de investigación. |
Panorama de inversión en descubrimiento de fármacos de IA
Después de 2021, el año anómalamente exitoso para la industria biotecnológica en términos de la cantidad de acuerdos de capital de riesgo, el número récord de ofertas públicas iniciales, una gran cantidad de salidas exitosas y un clima generalmente muy positivo en el mercado de valores, el año 2022 demostró un importante enfriamiento de la actividad financiera y un rotundo mal comportamiento de la bolsa.
Sin embargo, la inteligencia artificial en el sector del descubrimiento de fármacos demostró cierta resiliencia, al menos en el panorama de las transacciones de capital privado, con varias empresas recaudando cientos de millones en capital de riesgo. Algunos ejemplos incluyen MegaRobo Technologies con sede en Beijing ($300 millones Serie C), ConcertAI con sede en Massachusetts ($150 millones Serie C) y Celsius Therapeutics ($83 millones Serie A), Insilico Medicine con sede en Hong Kong ($95 millones Serie D), California- basado en BigHat Biosciences ($75 millones Serie B) y DeepCell ($73 millones Serie B), y varios otros - lea "Principales rondas de capital de riesgo para empresas de IA en descubrimiento de fármacos y biotecnología en 2022.
Un panorama de fusiones y adquisiciones estuvo marcado por un reciente acuerdo notable que involucró a un gigante de la biotecnología Ginkgo Bioworks adquiere Zymergen en una transacción que valora a Zymergen en 300 millones de dólares. La adquisición une las capacidades de ciencia de datos y aprendizaje automático de Zymergen con la plataforma de biología sintética de Ginkgo.
Observaciones y tendencias clave de la industria
El advenimiento de la inteligencia artificial y las tecnologías de datos, así como las nuevas herramientas informáticas y las soluciones de infraestructura (bases de datos, servicios en la nube, etc.), están redefiniendo la forma en que opera la industria farmacéutica, en los niveles de investigación, clínico y comercial. A continuación, revisemos algunas de las tendencias y observaciones en la IA para el espacio de descubrimiento de fármacos y desarrollos ilustrativos de la industria en 2022.
Modelado de biología habilitado por IA y descubrimiento de objetivos
En la investigación de descubrimiento de fármacos, la identificación de nuevos objetivos farmacológicos es fundamental para desarrollar nuevos fármacos terapéuticos de primera clase: posibles "éxitos de taquilla". Los esfuerzos de descubrimiento de fármacos durante varias décadas pasadas se centraron, tradicionalmente, en apuntar a proteínas específicas con "bolsillos" adecuados para ser influenciados por una molécula de ligando (a menudo, una molécula pequeña). Pero de la totalidad de todas las proteínas humanas (también conocidas como "proteoma"), se exploró una pequeña cantidad de proteínas como objetivos. Hay actualmente 20,360 proteínas humanas en Swiss-Prot, de las cuales se sabe que aproximadamente 4,600 están involucradas en los mecanismos de la enfermedad según la base de datos OMIM, lo que representa alrededor del 22 % de las proteínas humanas con funciones en la enfermedad. Estas proteínas son la región obvia del proteoma humano que probablemente contenga dianas farmacológicas viables. Sin embargo, como de 2017, solo alrededor de 890 biomoléculas humanas y derivadas de patógenos (principalmente proteínas) fueron realmente utilizadas por los medicamentos existentes aprobados por la FDA. Estas biomoléculas incluían 667 proteínas derivadas del genoma humano a las que se dirigen fármacos para enfermedades humanas. Las cosas no son muy diferentes hoy en día, por lo que todavía hay mucho espacio para identificar nuevos objetivos en este grupo. Los enfoques computacionales novedosos basados en tecnologías de inteligencia artificial permiten identificar nuevos bolsillos de proteínas susceptibles de fármaco a escala, lo que a veces permite pantallas virtuales de todo el proteoma.
Pero lo que es aún más emocionante, las herramientas de modelado avanzadas ayudan a identificar y modular nuevos tipos de objetivos, como interacciones proteína-proteína, objetivos con grandes áreas de contacto, interacciones proteína-ácido nucleico y objetivos de próxima generación, como la explotación de la proteína de la célula. maquinaria de degradación.
Muchas empresas impulsadas por IA se centran en modelar la biología, descubrir y validar nuevos objetivos y ofrecer "modelo de enfermedad como servicio" o "descubrimiento de objetivos como servicio" a otras organizaciones. La demanda de este tipo de servicios de investigación por contrato está aumentando, lo que se refleja en el creciente número de asociaciones de descubrimiento de objetivos.
Por ejemplo, en septiembre de 2022, una empresa de modelos biológicos con sede en Israel, CytoReason, anunció una colaboración ampliada de 110 millones de dólares con Pfizer. Las dos compañías comenzaron a trabajar juntas en 2019 cuando Pfizer comenzó a usar los modelos biológicos de CytoReason en investigaciones destinadas a desarrollar nuevos medicamentos para enfermedades inmunomediadas e inmunoterapias contra el cáncer.
En mayo de 2022, AstraZeneca anunció que recopiló un segundo objetivo de fibrosis pulmonar de su colaboración con BenevolentAI, un líder en el descubrimiento de fármacos impulsado por IA con sede en el Reino Unido. El hito marcó un tercer objetivo novedoso descubierto por BenevolentAI para AstraZeneca desde que comenzó la colaboración en 2019. Solo unos meses después, en octubre de 2022, BenevolentAI logró entregar dos objetivos adicionales generados por IA para la cartera de I + D de AstraZeneca, destinados a la enfermedad renal crónica y la enfermedad idiopática. fibrosis pulmonar.
En noviembre de 2022, Insilico Medicine, con sede en Hong Kong, firmó un acuerdo por un valor potencial de $ 1.2 millones con Sanofi para descubrir hasta seis nuevos objetivos que aprovechan la plataforma "Pharma.AI" de Insilico Medicine.
Si bien algoritmos de vanguardia como las redes neuronales profundas requieren grandes volúmenes de datos para modelar adecuadamente la biología, hay objetivos con una pequeña cantidad de datos disponibles. Cyclica, con sede en Canadá, desarrolló una plataforma impulsada por IA para la polifarmacología y la detección de todo el proteoma, capaz de trabajar con objetivos de "datos bajos". En noviembre de 2022, Cyclica recibió una subvención de 1.8 millones de dólares de la Fundación Bill y Melinda Gates para aplicar su plataforma de descubrimiento de fármacos habilitada por IA para descubrir nuevos contratos no hormonales, aprovechando múltiples objetivos biológicos de datos bajos.
Según el Informe de tendencias biofarmacéuticas, hay al menos otras 182 empresas de IA en el espacio de descubrimiento objetivo, incluidas empresas líderes bien financiadas con plataformas de investigación y desarrollo de vanguardia, como Insitro, Relay Therapeutics, Valo Health y otras.
Constantemente surgen nuevas empresas "nativas de IA" en el espacio de modelado de biología. Por ejemplo, CardiaTec Biosciences, WhiteLab Genomics, Degron Therapeutics, por nombrar algunos.
RELACIONADO: 11 Startups de descubrimiento de fármacos impulsadas por IA fundadas en 2021
En general, los métodos de modelado avanzados basados en inteligencia artificial ayudan a redefinir la definición misma de los objetivos biológicos, ya que tratamos de vincular la respuesta a los medicamentos con la variación genética, comprender la eficacia clínica estratificada y la seguridad, racionalizar las diferencias entre los medicamentos de la misma clase terapéutica y predecir utilidad del fármaco en subgrupos de pacientes.
Descifrando la biología estructural con IA
Uno de los temas relacionados con la IA más discutidos en la comunidad de ciencias de la vida este año fue el reciente éxito de DeepMind, la subsidiaria de Alphabet con sede en el Reino Unido, que recibió una amplia cobertura para su éxito en la resolución del problema de plegamiento de proteínas, un problema biológico de medio siglo de antigüedad.
En julio de 2022, el software de aprendizaje profundo AlphaFold de DeepMind predicho y compartido públicamente estructuras de proteínas de más de 200 millones de proteínas, habiendo demostrado la asombrosa capacidad de su sistema de IA para predecir con precisión estructuras 3D solo a partir de su secuencia de aminoácidos 1D. Si bien algunos argumentan que este descubrimiento puede no tener (todavía) un papel tan transformador en el descubrimiento de fármacos como se podría suponer, y que AlphaFold no se desempeñó mucho mejor que el azar al predecir las interacciones entre la proteína bacteriana y el compuesto antibacteriano, el descubrimiento es sin duda un cambio de paradigma tanto para la biología estructural como para ilustrar el potencial de la IA en la investigación biológica básica.
En noviembre de 2022, los investigadores de Meta (anteriormente Facebook, con sede en Menlo Park, California) rivalizaron con el éxito revolucionario de DeepMind en el modelado del proteoma. Usó IA para predecir las estructuras de unos 600 millones de proteínas de bacterias, virus y otros microorganismos que no han sido caracterizados.
Los científicos de Meta utilizaron un sistema completamente diferente enfoque de IA — usando un 'modelo de lenguaje grande', un tipo de IA que puede predecir texto a partir de unas pocas letras o palabras. Los modelos de lenguaje natural (NLP) generalmente se entrenan en grandes volúmenes de texto. Sin embargo, las secuencias de proteínas 1D son esencialmente cadenas de letras, por lo que los NLP se pueden aplicar a tales problemas de manera similar a trabajar con lenguajes humanos.
Curiosamente, estos importantes avances tecnológicos en el plegamiento de proteínas podrían resultar más útiles para diseño de proteínas de novo, que simplemente modelar estructuras de proteínas existentes para el descubrimiento de fármacos. El tiempo dirá dónde será mayor el impacto, pero los éxitos anteriores de DeepMind y Meta no son el único desarrollo emocionante para los biólogos estructurales en 2022.
Recientemente, los rápidos avances en crio-EM, junto con las tecnologías de IA, dieron origen a una nueva ola de nuevas empresas de biotecnología como Gandeeva Therapeutics, Septerna y MOMA Therapeutics. El campo de la crio-EM se está calentando con las nuevas empresas de biotecnología que atraen la atención de una amplia gama de inversores, desde las organizaciones de riesgo más pequeñas hasta el propietario de TikTok y el gigante tecnológico de Internet ByteDance, que invierte en Shuimu BioSciences. El interés está impulsado no solo por la revolucionaria tecnología ganadora del premio Nobel, sino también por el reclutamiento activo de IA en el proceso. La reciente publicación “Una tubería crio-EM asistida por IA para estudios estructurales de extractos celulares” destacó el papel no reemplazable de la IA en procesos crio-EM complejos, incluida la predicción de modelos atómicos impulsados por IA para investigar rápida y simultáneamente la estructura de múltiples miembros de la comunidad de proteínas de novo. El aprendizaje automático ayuda no solo a acelerar y optimizar la tubería crio-EM, sino también a evitar las trampas del sesgo del usuario.
Gandeeva Therapeutics, fundada en 2021, recaudó 40 millones de dólares a principios de este año para desarrollar terapias novedosas basadas en imágenes de precisión de interacciones entre proteínas y fármacos. Su motor de selección de objetivos junto con el motor Cryo-EM pueden ayudar a "alejarse de los callejones sin salida del descubrimiento", como afirmó la compañía. Al mismo tiempo, con el lanzamiento en 2020 de la biotecnología cryo-EM, MOMA Therapeutics recaudó la friolera de $ 236 millones en solo dos años, con el ambicioso objetivo de lanzar a la clínica nuevos medicamentos de precisión para el cáncer. MOMA se centra en una clase única de objetivos biológicos: "máquinas moleculares".
Desarrollo de moléculas pequeñas usando IA
Después del modelado de enfermedades y el descubrimiento de objetivos, el diseño de moléculas químicas o biológicas es el segundo caso de uso más abundante para aplicar la inteligencia artificial en el descubrimiento de fármacos. Más de 130 empresas impulsadas por inteligencia artificial de las 384 empresas en el informe BiopharmaTrend AI aplican inteligencia artificial para diseñar candidatos a fármacos, entre otros casos de uso.
El diseño de fármacos impulsado por IA se divide principalmente en tres categorías principales: diseño de fármacos de novo (por ejemplo, generativo), cribado virtual de bases de datos existentes y reutilización de fármacos.
El diseño de fármacos de novo está habilitado principalmente por modelos de aprendizaje profundo, como las redes neuronales antagónicas generativas (GAN). Algunos ejemplos de plataformas de IA generativa incluyen el software Chemistry42 de Insilico Medicine, Makya de Iktos y De Novo Platform de Ro5. Otros jugadores en esta categoría incluyen Recursion Pharmaceuticals, Deep Cure, Standigm y otros.
La aplicación de detección virtual a gran escala habilitada por inteligencia artificial, examinando miles de millones de moléculas para encontrar resultados exitosos. En agosto de 2022, Sanofi se asoció con Atomwise en un acuerdo de diseño de fármacos con un valor potencial de hasta 1.2 millones de dólares. El acuerdo, en el que Sanofi pagará 20 millones de dólares por adelantado, se centra en aprovechar la plataforma AtomNet de la compañía estadounidense para investigar moléculas pequeñas para hasta cinco objetivos farmacológicos seleccionados por Sanofi. Una AtomNet basada en una red neuronal convolucional sobresale en el diseño de fármacos basado en la estructura, lo que permite "la búsqueda rápida impulsada por IA de la biblioteca patentada de Atomwise de más de 3 billones de compuestos sintetizables", según el anuncio.
A principios de 2019, Atomwise colaboró con el líder químico con sede en Ucrania, Enamine, para realizar la "primera y más grande pantalla virtual de 10 mil millones de compuestos del mundo", con el objetivo de identificar éxitos para la oncología pediátrica.
Finalmente, varias empresas están utilizando estrategias de reutilización para el descubrimiento de fármacos habilitados por IA. Las empresas en esta categoría, incluidas Healx, BenevolentAI, BioXcel Therapeutics, utilizan en gran medida modelos de procesamiento de lenguaje natural (NLP) y aprendizaje automático y operan mediante el análisis de cantidades masivas de datos textuales no estructurados: artículos de investigación y patentes, registros de salud electrónicos (EHR), como así como otros tipos de datos, para construir y buscar "gráficos de conocimiento". Dichas ontologías de búsqueda habilitadas para IA permiten seleccionar indicaciones novedosas o poblaciones de pacientes para candidatos a fármacos previamente conocidos o incluso fármacos aprobados.
Por ejemplo, Lantern Pharma, una empresa de biotecnología en etapa clínica con sede en EE. UU., se centró en innovar el proceso de desarrollo de fármacos contra el cáncer mediante el uso de genómica avanzada, aprendizaje automático e inteligencia artificial.
La plataforma de IA de la compañía, RADR®️, actualmente incluye más de 25 XNUMX millones de puntos de datos y utiliza análisis de big data y aprendizaje automático para descubrir rápidamente firmas genómicas biológicamente relevantes correlacionadas con la respuesta a los medicamentos, y luego identificar subgrupos de pacientes con cáncer relevantes para beneficiarse de los candidatos a fármacos de Lantern. . RADR ®️ también es utilizado por Lantern y sus colaboradores para desarrollar y posicionar nuevos medicamentos, así como para la reutilización de medicamentos.
RELACIONADO: Presentación de la historia de éxito de Lantern Pharma en oncología de precisión impulsada por IA
La IA se encuentra con las bibliotecas codificadas por ADN
Un enfoque algo único para el diseño de fármacos consiste en utilizar bibliotecas codificadas por ADN (DEL) como fuente de nuevas moléculas para buscar. Dado que la tecnología DEL ofrece acceso esencialmente al espacio químico más grande disponible en el mercado, esta tecnología de big data se adapta naturalmente a las herramientas basadas en IA.
Un notable acuerdo tuvo lugar en 2020, cuando Insitro, uno de los actores destacados en la aplicación del aprendizaje automático para el descubrimiento de fármacos, fundado por Daphne Koller, adquirió Haystack Sciences. La plataforma basada en el aprendizaje automático de Haystack combinó múltiples elementos de su tecnología DEL, incluida la capacidad de sintetizar colecciones de moléculas pequeñas amplias y diversas, la capacidad de ejecutar un seguimiento iterativo y una tecnología de detección semicuantitativa patentada llamada nDexer™, que genera conjuntos de datos de mayor resolución.
A su vez, ZebiAI fue adquirida en 2021 por otro desarrollador notable de una plataforma de descubrimiento de fármacos impulsada por inteligencia artificial, Relay Therapeutics de biotecnología en etapa clínica, donde Relay pagó $ 85 millones por adelantado. Esta adquisición permitió a Relay incorporar la tecnología DEL basada en aprendizaje automático de ZebiAI en su plataforma de orientación de proteínas Dynamo.
RELACIONADO: Una revisión de mercado de la tecnología de bibliotecas codificadas por ADN en el descubrimiento de fármacos
En octubre de 2021, X-Chem adquirió Glamorous AI, un desarrollador de una solución modular de inteligencia artificial multifacética para el descubrimiento de fármacos RosalindAI, que incluye capacidades de ingeniería y caracterización de datos, análisis predictivo, computación de alto rendimiento y diseño de fármacos de novo.
Diseño de fármacos impulsado por IA más allá de las moléculas pequeñas
Teniendo en cuenta que las herramientas de inteligencia artificial de hoy en día aplicadas para el descubrimiento de fármacos tienen profundas raíces históricas en la quimioinformática y los primeros modelos QSAR basados en el aprendizaje automático del siglo pasado, no sorprende que la gran mayoría de las nuevas empresas de IA en el descubrimiento de fármacos se centren en moléculas pequeñas. .
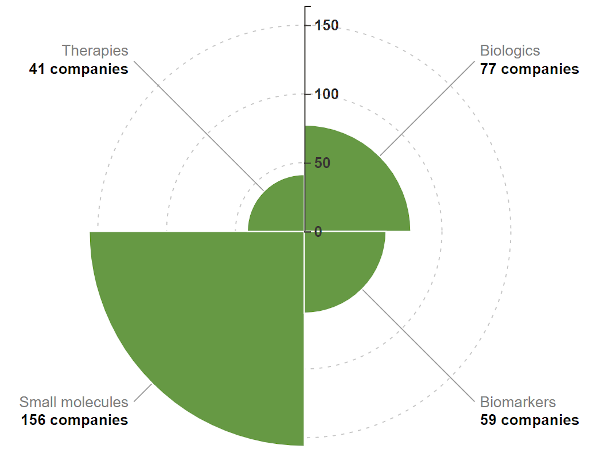
Distribución de empresas de descubrimiento de fármacos de IA por categoría de producto. Fuente: Informe de IA de BiopharmaTrend.
Sin embargo, los medicamentos de biomoléculas (también conocidos como "biológicos") y las nuevas modalidades químicas son cada vez más abundantes en el espacio farmacéutico, al igual que las nuevas empresas de biotecnología que aplican métodos basados en IA para descubrirlos. Después de que los científicos descifraran el genoma humano en 2003, el espacio de farmacabilidad y desarrollo evolucionó rápidamente. En el siglo pasado, la regla de cinco de Lipinski (Ro5) solía servir como una "luz de guía" para el diseño de moléculas similares a fármacos para la administración oral en el espacio de destino farmacológico "tradicional".
Por el contrario, los nuevos tipos de objetivos, como las interacciones proteína-proteína, los objetivos con grandes áreas de contacto, las interacciones proteína-ácido nucleico y los objetivos de próxima generación, como la explotación de la maquinaria de degradación de proteínas de las células, están impulsando el advenimiento de una variedad de tecnologías emergentes. modalidades moleculares, es decir, más allá de las moléculas pequeñas Ro5 (bRo5) (como los moduladores de la interacción proteína-proteína, las quimeras dirigidas a proteínas (PROTAC), los anticuerpos monoclonales (mAb), los péptidos y los peptidomiméticos, y las modalidades basadas en ácidos nucleicos (ARN y ADN- basado), se han convertido en un foco clave en el descubrimiento de fármacos.
RELACIONADO: La “explosión” de las modalidades terapéuticas: moléculas pequeñas, productos biológicos y todo lo demás,
Por ejemplo, hay un número creciente de empresas que aplican métodos de IA para descubrir nuevos anticuerpos monoclonales, la modalidad biológica de mayor éxito comercial hasta el momento. En particular, en abril de 2022, Biolojic Design, con sede en Israel, anunció su primer anticuerpo diseñado computacionalmente. entró en el ensayo clínico. La empresa aprovecha una estrategia de diseño basada en la estructura. Su modelo de IA está entrenado en millones de pares de anticuerpos y antígenos para identificar un anticuerpo molde contra el objetivo de interés de los anticuerpos humanos existentes. Se utiliza un modelo de aprendizaje automático adicional para predecir mutaciones y guiar la optimización de la plantilla para mejorar sus propiedades.
En noviembre de 2022, AbCellera Biologics, con sede en Canadá, anunció que Regeneron eligió ejercer su derecho a avanzar en el desarrollo preclínico del primero de los candidatos a anticuerpos terapéuticos de AbCellera dirigidos a un receptor acoplado a proteína G (GPCR) no revelado. La asociación, que comenzó en marzo de 2020 y permite cuatro programas de descubrimiento seleccionados por Regeneron, aprovecha el motor de descubrimiento de anticuerpos basado en IA de AbCellera y los ratones VelocImmune® de Regeneron para identificar nuevos anticuerpos terapéuticos.
Otras dos docenas de empresas de descubrimiento de anticuerpos están utilizando IA, incluidas AbSci, BigHat Biosciences, Totient, Nabla Bio y Generate Biomedicine, con sede en EE. UU.; Deep Biologics, con sede en Canadá; NeoX con sede en China; Deep CDR, Natural Antibody y MabSilico, etc., basados en la UE.
La empresa con sede en EE. UU. con un nombre pegadizo Creyon Bio aplica un enfoque de ingeniería para crear nuevos medicamentos basados en oligonucleótidos (OBM). La empresa se fundó en 2019 y recaudó 40 millones de dólares en fondos en marzo de 2022. Fundada en 2014 como una escisión de Cold Spring Harbor Laboratory, Envisagenics es una empresa con sede en Nueva York que se centra en el descubrimiento de terapias de ARN. De acuerdo con su misión declarada, su objetivo es reducir la complejidad de los datos biomédicos con la ayuda de tecnologías AI/ML. Recientemente, en agosto de 2022, recibieron una subvención del Instituto Nacional del Cáncer, lo que resultó en una financiación total recaudada de $27.1 millones.
La tecnología impulsada por IA de Envisagenics, SpliceCore, es una plataforma basada en la nube validada experimentalmente para predecir objetivos farmacológicos y biomarcadores a través del descubrimiento de empalmes a partir de datos de secuenciación de ARN. Según la empresa, asegura una mayor precisión y velocidad en comparación con los métodos tradicionales.
La estrategia impulsada por la IA de Innophore para diseñar enzimas terapéuticas novedosas se realiza mediante el acoplamiento de su tecnología Catalophore™ patentada con enfoques bioinformáticos convencionales de última generación e inteligencia artificial. Innophore puede extraer bases de datos estructurales y de secuencias utilizando plantillas de búsqueda tridimensionales (3D) llamadas "catalóforos" (es decir, portadores de la función catalítica) definidos por nubes de puntos de características fisicoquímicas. Las nuevas enzimas identificadas por esta técnica no necesariamente comparten una estructura común o una base de secuencia con sus contrapartes empleadas. Por lo tanto, presentan potencialmente propiedades proteicas alteradas, como termoestabilidad, robustez, espectro de sustrato, selectividad y especificidad.
Además de diseñar nuevas enzimas, la tecnología de Innophore puede potencialmente cambiar las reglas del juego para aplicaciones epidemiológicas, protegiendo mutaciones potencialmente peligrosas en virus. En 2021, Innophore inició el proyecto virus.watch en cooperación con la Iniciativa de desarrollo de diagnóstico de AWS. El objetivo de este proyecto fue la implementación de un sistema de monitoreo y evaluación para variantes de coronavirus (SARS-CoV-2) emergentes y relevantes para enfermedades. El primer documento conjunto, publicado en Nature en agosto de 2022, describe el análisis bioinformático de las variantes del SARS-CoV-2 que revelan una mayor afinidad de unión al receptor hACE2 por el pico RBD de Omicron B.1.1.529 en comparación con una referencia de tipo salvaje.

El seguimiento de la evolución del virus a lo largo del tiempo utilizando la tecnología Innophore y AWS muestra una alta tasa de mutaciones que surgen con la variante Omicron. Las esferas representan átomos de alfa-C del residuo de aminoácido correspondiente. Tanto el color como el tamaño se correlacionan con el número de mutaciones en cada posición.
Fundada en 2008, Evaxion Biotech, con sede en Dinamarca, es una empresa impulsada por la IA, dedicada al desarrollo de vacunas contra el cáncer y las enfermedades infecciosas. Poseen una plataforma de inmunología de IA de etapa clínica, que combina la tecnología de IA con su experiencia en ingeniería para generar modelos predictivos, lo que ayuda a identificar inmunoterapias únicas para los pacientes. Evaxion Biotech atrajo un total de $ 57 millones, ingresando a la ronda de financiación de capital posterior a la OPI en junio de 2022 por un valor de $ 40 millones, liderada por un solo inversor Lincoln Park Capital Fund.
RELACIONADO: 10 empresas que aplican IA para diseñar productos biológicos
Algunas empresas de IA del “club de modalidades químicas”, como Exscientia, ahora se están expandiendo al descubrimiento de productos biológicos. En noviembre de 2022, la empresa anunció que su plataforma de IA incluiría el diseño de anticuerpos humanos. Exscientia también está estableciendo un laboratorio biológico automatizado en Oxford para generar internamente y perfilar nuevos anticuerpos.
Una tendencia creciente es explotar el sistema de degradación de proteínas de las células humanas para deshacerse de las proteínas malignas y curar enfermedades. Una modalidad aquí que está aumentando en popularidad es la quimera dirigida a la proteólisis (PROTAC) que se introdujo en 2001 y consta de dos ligandos conectados por un conector flexible. La arquitectura química principal de los PROTAC modernos es la misma: un ligando se dirige a la enzima E3, que es un componente que envía proteínas obsoletas al proteasoma, y otro ligando se dirige a una proteína de interés (POI) que debe degradarse. Un PROTAC se une a E3 y POI, acercándolos para formar un complejo de proximidad inducida. En algunos casos, cuando las proteínas se alinean correctamente, el PDI se ubiquitina, lo que lo marca para que el proteosoma lo degrade.
Otro enfoque amplio de la degradación de proteínas incluye los llamados "pegamentos moleculares", un área de investigación en constante crecimiento. A diferencia de los PROTAC, que son moléculas pequeñas bifuncionales relativamente grandes con dos sitios activos y un enlazador, los adhesivos moleculares son moléculas más pequeñas y más parecidas a fármacos. Estos últimos se unen a un bolsillo de proteína agregada que resulta de dos proteínas separadas que se acercan debido al efecto de la molécula de pegamento molecular.
Hay una ola de compañías dentro del espacio de la degradación de proteínas (y, más ampliamente, de la modulación), que incluyen Arvinas, Terapéutica Nurix, Terapéutica Kymera, C4 Therapeutics, Roivant Discovery, Cedilla Therapeutics y Lycia Therapeutics, por nombrar algunos.
Algunas empresas están aplicando algoritmos de inteligencia artificial de vanguardia para diseñar compuestos que inducen proximidad. Por ejemplo, Celeris Therapeutics, con sede en Austria y EE. UU., ha construido la plataforma Celeris One, que incluye tres sistemas de zona de trabajo: Xanthos, Hephaistos y Hades. Los sistemas incorporan redes neuronales gráficas para predecir interacciones y modelos generativos para crear nueva materia química, como enlazador y optimización multiobjetivo para mejorar las propiedades moleculares, la dinámica molecular y los cálculos de energía libre. El flujo de trabajo también emplea el aprendizaje profundo geométrico y las capacidades de retrosíntesis impulsadas por el aprendizaje automático. Celeris Therapeutics tiene un laboratorio automatizado para generar datos biológicos y realizar síntesis químicas personalizadas.

El flujo de trabajo del laboratorio seco de la plataforma impulsada por IA Xanthos de Celeris Therapeutics.
Recientemente hemos publicado una amplia descripción del mercado de degradación de proteínas en una publicación Los degradadores de proteínas conquistan la industria, incluidos varios estudios de casos con una descripción técnica de las plataformas computacionales involucradas.
La primera ola de candidatos a fármacos desarrollados por IA se vuelve clínica
Si bien es probable que sea pronto para decir que la adopción de la IA en la industria farmacéutica revolucionó por completo el descubrimiento de fármacos, varias empresas "nativas de la IA" lograron obtener una eficiencia notable en la construcción rápida de sus proyectos terapéuticos. ¿Cuál es una característica común de tales empresas? Cada uno creó una plataforma de IA especializada y altamente integrada, que incluye muchos modelos y fuentes de datos. Algunas plataformas también están disponibles como software como servicio para socios externos de I+D, como Chemistry42.
Uno de los ejemplos más vívidos de beneficiarse de una estrategia de "primero lo digital" que ha visto la industria es Moderna Therapeutics, que no solo logró incorporar análisis de IA de vanguardia en su investigación, sino que digitalizó e integró todos los aspectos de su flujo de trabajo de I+D, incluidos producción y distribución. Cuando la pandemia de COVID-19 golpeó al mundo a principios de 2020, Moderna fue una de las primeras empresas en poder crear una vacuna eficiente basada en ARNm en solo 2 días (!) y llevarla al mercado en un año. .
Una ola de éxitos en el descubrimiento de terapias gracias a la IA demuestra la capacidad de las empresas nativas de la IA para encontrar candidatos a fármacos más rápido de lo que solían tardar programas similares.

Ver “La hoja de ruta de los candidatos a fármacos diseñada por IA”
El anticuerpo monoclonal LY-CoV555 de AbCellera se desarrolló en tres meses y obtuvo la autorización de uso de emergencia de la FDA.
Knowledge Graph de BenevolentAI ayudó a la compañía a identificar a Baricitinib como un antiviral COVID-19 eficiente en cuestión de días (ahora aprobado para su uso por la FDA). Otra molécula pequeña BEN-8744, un nuevo inhibidor para tratar la colitis ulcerosa y la dermatitis, avanzó a estudios preclínicos tardíos en menos de 24 meses.
El inhibidor de molécula pequeña EXS-21546 de Exscientia marcó la primera molécula diseñada por IA para inmuno-oncología en ingresar a ensayos clínicos en humanos (ahora en Fase I) y se descubrió en solo ocho meses. La compañía tiene varias otras moléculas en ensayos clínicos.
El inhibidor de molécula pequeña ISM001-055 de Insilico Medicine, para tratar la fibrosis pulmonar idiopática, se diseñó de novo y avanzó en estudios preclínicos tardíos en 18 meses (ahora en Fase I).
Schrodinger, con sede en Nueva York, desarrolló una molécula pequeña SGR-1505 para tratar el linfoma de células B en diez meses y ahora está en proceso de aplicación IND.
Recursion Pharmaceuticals, con sede en Salt Lake City, desarrolló un fármaco candidato para una enfermedad rara no especificada en 18 meses. La compañía tiene una cartera grande y diversa de candidatos a fármacos preclínicos y clínicos diseñados con la ayuda de su plataforma de biología digital.
Deep Genomics, con sede en Toronto, utilizó su plataforma AI Workbench para desarrollar un objetivo genético novedoso y un candidato a fármaco oligonucleótido correspondiente, DG12P1, para tratar una rara enfermedad hereditaria de Wilson.
Para realizar un seguimiento de los principales candidatos a fármacos clínicos desarrollados por IA, hemos creado “La hoja de ruta de los candidatos a fármacos diseñada por IA” que se actualizará periódicamente.
Cabe señalar que la atención de los medios en curso a la IA para el descubrimiento de fármacos debe considerarse a través de una lente de precaución. Por ejemplo, el plan de BenevolentAI para obtener la licencia de su candidato a fármaco para la dermatitis atópica, BEN-2293, sufrió un revés ya que el inhibidor pan-Trk habilitado para IA no logró mejorar los síntomas del eccema o la picazón en un ensayo de fase 2a. La empresa había identificado previamente los receptores quinasas de tropomiosina (Trk) como mediadores del picor y la inflamación en la dermatitis atópica, lo que condujo al desarrollo de inhibidores de Trk. Aunque BEN-2293 demostró una tendencia hacia un efecto clínicamente significativo en un ensayo de fase 1b, el ensayo de fase 2a reveló que no era mejor que un placebo para mejorar la gravedad del eczema o la picazón. El resultado plantea preguntas sobre la plataforma habilitada para IA que propuso el enfoque. A pesar del contratiempo, BenevolentAI no ha renunciado al candidato a fármaco, citando evidencia de que el tratamiento funcionó mejor en pacientes con una mayor extensión de la enfermedad al inicio del estudio. La compañía actualmente está revisando los datos antes de determinar sus próximos pasos.
Las veinte empresas de IA más "productivas" en el espacio de descubrimiento de fármacos
Después de haber preseleccionado alrededor de 130 empresas de más de 380 empresas de IA en el Informe de IA de BiopharmaTrend, hemos seleccionado otras 20 empresas, utilizando una fórmula de evaluación simple pero sólida que tiene en cuenta los proyectos clínicos y preclínicos de las empresas, la capacidad para el descubrimiento de objetivos y el tiempo. en los negocios. Las 20 empresas seleccionadas formaron el BPT20: índice de productividad de inteligencia artificial en el descubrimiento de fármacos — el primer punto de referencia de la industria para destacar a las empresas que defienden la aplicación de la IA para el diseño de fármacos de novo, la detección virtual o la reutilización de fármacos.

IA y laboratorios robotizados del futuro
Los modelos de aprendizaje profundo (p. ej., basados en redes neuronales profundas) son extremadamente "hambrientos de datos", lo que significa que no importa cuán buena sea la IA, la calidad y el tamaño de los datos son igualmente importantes para las predicciones de investigación significativas. La forma más eficiente de generar datos biológicos de alta calidad es mediante el uso de robótica. Si consideramos la transformación moderna impulsada por la IA del descubrimiento de fármacos como un proceso paso a paso, ampliamente disponible y relativamente rentable rOBotics-as-a-Service sería la pieza final y crítica en la IA habilitada industrialización de la investigación farmacéutica y biotecnológica. Según un informe de Arctoris, "La robótica es clave para permitir que el paradigma del descubrimiento de circuito cerrado se convierta en realidad, que será un espacio emocionante para observar en los próximos años".
Algunas empresas están construyendo instalaciones de laboratorio estandarizadas, altamente automatizadas, escalables y cada vez más compatibles guiadas por sistemas de control de experimentos basados en IA y complementadas con capacidades de análisis y minería de datos impulsadas por IA. Estas instalaciones de laboratorio de "próxima generación" están disponibles de forma remota para los experimentadores de investigación preclínica de medicamentos, lo que hace que la experimentación preclínica sea una rutina más escalable y estandarizada. Los principales proveedores de laboratorios remotos de la lista son Automata Labs, Strateos, Emerald Labs y Culture Biosciences, por nombrar algunos.
El espacio está atrayendo financiación de riesgo y clientes. Por ejemplo, en febrero de 2022, Automata Labs, con sede en el Reino Unido, recaudó 50 millones de dólares para automatizar el proceso de investigación de laboratorio. En julio de 2021, Strateos recaudó $ 56 millones para mejorar aún más su plataforma SmartLab y su tecnología automatizada y robotizada remota, disponible para investigadores preclínicos de todo el mundo. Culture Biosciences recaudó un total de más de $ 100 millones, con la última Serie B de $ 80 millones anunciada en noviembre de 2021. Emerald Cloud Labs (ECL), con sede en San Francisco, recaudó más de $ 90 millones a lo largo de los años. Primeros usuarios de la plataforma robótica remove de ECL informó mejoras del 300 % al 700 % en la productividad de la investigación. En junio de 2022, MegaRobo, con sede en Beijing, recaudó $ 300 millones para expandir su diversa gama de servicios de laboratorio remoto automatizados e instalaciones robotizadas impulsados por IA.
El auge de los laboratorios robotizados remotos es una tendencia de la industria a largo plazo, una nueva forma de ofrecer servicios de investigación por contrato que sería extremadamente beneficioso para la adopción a largo plazo de estrategias de investigación centradas en los datos "AI-first".
Varias compañías de descubrimiento de fármacos impulsadas por IA, como Arctoris, Recursion Pharmaceuticals, Insitro y Generative Bio, se están acercando a esta tendencia a través de un modelo comercial diferente: han construido instalaciones de laboratorio robotizadas internas para mejorar sus capacidades internas de generación de datos para capacitar a sus Modelos de IA y desarrollo de proyectos de candidatos a fármacos terapéuticos.
Por ejemplo, Arctoris, con sede en Oxford, fundada en 2016, construyó un laboratorio húmedo totalmente automatizado que genera datos de calidad superior a escala, alimentando el lago de datos de Arctoris y potenciando la plataforma de toma de decisiones impulsada por IA de la empresa, Ulysses, que impulsa la investigación de la empresa desde objetivo para golpear, liderar y para la etapa de aplicación IND.
La cartera de proyectos de Arctoris ahora incluye varios programas preclínicos en oncología y neurología. Arctoris recaudó un total de 10.3 millones de dólares en varias rondas de inversores, incluidos Future Planet Capital, RT Ventures y Formic Ventures.
Algunas empresas líderes en el descubrimiento de fármacos de IA, como Exscientia e Insilico Medicine, ahora también están construyendo laboratorios robotizados internos para desarrollar sus "músculos" internos de generación de datos.
Recursion Pharmaceuticals, con sede en Salt Lake City, se encuentra entre los líderes en el espacio de experimentación de biología robotizada. La infraestructura impulsada por IA de la compañía, llamada Recursion Operation System, es un sistema integrado de circuito cerrado que combina la generación de datos internos patentados y herramientas computacionales avanzadas para generar conocimientos novedosos para iniciar o acelerar programas terapéuticos. La empresa está automatizando la experimentación biológica preclínica a escala. Por ejemplo, las imágenes de microscopía celular capturan cambios compuestos en la morfología celular y son procesadas por los sistemas de visión por computadora impulsados por inteligencia artificial de la compañía. Desde 2017, Recursion Pharmaceuticals ha duplicado aproximadamente la capacidad de la plataforma fenómica cada año y escaló la cantidad de experimentos fenómicos ejecutados hasta 2.2 millones por semana, lo que da como resultado ~19 petabytes de datos patentados de alta dimensión.
Navegar por los cuellos de botella de los ensayos clínicos con IA
El ensayo clínico es una etapa crítica del flujo de trabajo de desarrollo de fármacos, con una tasa de éxito promedio estimada de aproximadamente 11% para fármacos candidatos que pasan de la Fase 1 a la aprobación. Incluso si el fármaco candidato es seguro y eficaz, los ensayos clínicos pueden fallar debido a financiamiento insuficiente, inscripción insuficiente o diseño de estudio deficiente.
La Inteligencia Artificial (IA) es cada vez más percibida como una fuente de oportunidades para mejorar la eficiencia operativa de los ensayos clínicos y minimizar los costos de desarrollo clínico. Por lo general, los proveedores de IA ofrecen sus servicios y experiencia en tres áreas principales. Las nuevas empresas de IA en la primera área ayudan a desbloquear información de fuentes de datos dispares, como artículos científicos, registros médicos, registros de enfermedades e incluso declaraciones médicas, mediante la aplicación de procesamiento de lenguaje natural (NLP). Esto puede respaldar el reclutamiento y la estratificación de pacientes, la selección de sitios y mejorar el diseño de estudios clínicos y la comprensión de los mecanismos de la enfermedad. A modo de ejemplo, alrededor del 18 % de los estudios clínicos fracasan debido a un reclutamiento insuficiente, como un estudio de 2015 informó.
Otro aspecto del éxito en los ensayos clínicos es la estratificación mejorada de los pacientes. Dado que los pacientes del ensayo son costosos, el costo promedio de inscribir a un paciente fue $ 15,700-26,000 en 2017: es esencial poder predecir qué paciente tendrá un beneficio o riesgo más significativo del tratamiento. Las empresas impulsadas por IA operan con múltiples tipos de datos, como registros médicos electrónicos (EHR), ómicas y datos de imágenes, para reducir la heterogeneidad de la población y aumentar el poder de los estudios clínicos. Los proveedores podrían usar biomarcadores del habla para identificar la progresión de la enfermedad neurológica, análisis de imágenes para rastrear la progresión del tratamiento o biomarcadores genéticos para identificar pacientes con síntomas más graves.
AI también está simplificando los procesos operativos de los ensayos clínicos. Los proveedores de IA ayudan a rastrear la salud del paciente desde sus hogares, monitorear la respuesta al tratamiento y la adherencia del paciente a los procedimientos del ensayo. Al hacer eso, las empresas de IA reducen el riesgo de abandono de los pacientes, lo que explica 30% de media. Por lo general, la etapa de estudio clínico de Fase 3 requiere 1000 - 3000 participantes, con una parte de ellos tomando un placebo. Por eso el desarrollo de brazos de control sintéticos – Los modelos de IA que podrían reemplazar a los grupos de individuos con control de placebo, reduciendo así la cantidad de individuos necesarios para los ensayos clínicos, podrían convertirse en una tendencia novedosa.
Hay más de 80 empresas en las tres categorías, según el informe BiopharmaTrend AI, incluidas Owkin, PathAI, GNS Healthcare, Neurcuit, AICure y Unlearn.ai.
RELACIONADO: 8 empresas notables de IA en investigación clínica para observar en 2022
La demanda de plataformas de ensayos clínicos habilitadas para IA es alta, así como las inversiones en esta área, a pesar del frío clima general de inversión en biotecnología.
En marzo de 2022, ConcertAI obtuvo una valoración de $ 1.9 mil millones después de depositar una ronda de serie C de $ 150 millones para escalar sus soluciones de software y datos del mundo real (RWD) para la investigación del cáncer.
Saama es una empresa con sede en Silicon Valley fundada en 1997, pero recaudó su primer capital de riesgo en 2015. La empresa ha recaudado más de $500 millones en capital de riesgo, incluida la última mega ronda de $430 millones en agosto de 2022, de Carlyle y fondos de riesgo de Merck, Pfizer, Amgen, McKesson y otros.
Saama es uno de los actores líderes en el espacio de análisis de ensayos clínicos impulsados por IA y ofrece un conjunto diverso de soluciones: ensayos clínicos acelerados a través de un centro de control y análisis de datos centralizados, que incluye capacidades de procesamiento de datos en tiempo real; capacidades de calidad de datos automatizados; Capacidades simplificadas de envío regulatorio, incluidos análisis y envíos de farmacovigilancia.
En abril de 2022, Unlearn.AI, una startup que desarrolla un servicio de "gemelo digital" para ensayos clínicos, recaudó 50 millones de dólares.
En junio de 2022, Bristol Myers Squib invirtió $ 80 millones en OWKIN, para ayudar a mejorar el diseño de ensayos de medicamentos cardiovasculares, con mejoras en las definiciones de los criterios de valoración, la identificación de subgrupos de pacientes y la estimación de los efectos del tratamiento. OWKIN, el “unicornio” con sede en París y Nueva York, está aprovechando nuestro acceso a datos multimodales de alta calidad y el aprendizaje automático de última generación para predecir con precisión varios efectos del tratamiento en subpoblaciones de pacientes para mejorar el diseño y los resultados de los experimentos de ensayos clínicos. OWKIN también está aplicando su plataforma de IA para el descubrimiento de fármacos.
En agosto de 2022, Bristol Myers Squibb también anunció un acuerdo de colaboración ampliado de varios años con el especialista en patología de IA PathAI. El trabajo inicial dentro de este acuerdo ampliado se centrará en la investigación traslacional clave en oncología, fibrosis e inmunología, con el objetivo general de enviarlos a ensayos clínicos. Dos meses antes, PathAI estableció una asociación estratégica de varios años con GlaxoSmithKline para acelerar la investigación científica y los programas de desarrollo de fármacos en oncología y esteatohepatitis no alcohólica (NASH) aprovechando las tecnologías de PathAI en patología digital, incluido el uso de la herramienta AIM-NASH de PathAI.
En particular, Akkure Genomics de Dublín acaba de anunciar financió 1 millón de euros en una semana para apoyar los ensayos clínicos a través de su plataforma de IA, que ayuda a las personas a participar en los ensayos clínicos más relevantes basados en datos sobre ellos mismos y su condición.
IA en la industria de la investigación por contrato
La aparición de nuevas empresas de investigación por contrato nativas de IA en espacios preclínicos y clínicos desafía el status quo de las principales organizaciones de investigación por contrato (CRO) bien establecidas. Responden incorporando IA en sus ofertas de servicios a la industria farmacéutica o asociándose con empresas de IA para complementar su capacidad de investigación.
RELACIONADO: La evolución de la industria de subcontratación de I+D farmacéutica: una vista panorámica.
Por ejemplo, Charles River Labs, una organización de investigación por contrato en etapa inicial con sede en EE. UU., está profundizando en la IA mediante el establecimiento de un asociación de varios años con Valo Health. Charles River agrega la tecnología Opal de Valo que aprende activamente a medida que se desarrollan los programas. Charles River espera que el uso de la plataforma de aprendizaje profundo Opal resulte en un proceso más rápido y efectivo desde el diseño de moléculas de novo hasta la optimización de los líderes. El año pasado, Charles River estableció una asociación estratégica con Valence Discovery que permitió a los clientes de la CRO acceder a la plataforma de inteligencia artificial de Valence para la predicción de propiedades moleculares, la química generativa y la optimización multiparamétrica.
IQVIA ha estado invirtiendo en capacidades de IA durante años para agregar valor a los ensayos clínicos y las actividades comerciales que ofrece a los clientes. Para mejorar los ensayos clínicos, por ejemplo, IQVIA lanzado Avacare Clinical Research Network™ en 2020, lo que permitió a los sitios unir a los pacientes para los ensayos de manera más rápida y eficiente. La plataforma funciona con algoritmos de IA y puede operar en 19 áreas de enfermedades. Anteriormente, otra plataforma Linguamatics Natural Language Processing (NLP) de IQVIA ganó los Fierce Innovation Awards 2019 de Questex. La plataforma puede tener amplias aplicaciones en el cuidado de la salud y las ciencias de la vida, incluida la identificación de objetivos, el mapeo de genes, la predicción de los resultados de los pacientes, etc.
Se está produciendo una tendencia significativa en la industria de la investigación clínica ensayos clínicos virtuales, un mercado valorado en 8 millones de dólares. La pandemia de COVID-19 obligó a las empresas farmacéuticas a cambiar a la monitorización remota, mejorar la inscripción de pacientes, aplicaciones para realizar un seguimiento de la participación de los pacientes, la telemedicina, la descentralización y otras medidas para mantener los ensayos en marcha. Dado que la demanda de tales soluciones creció significativamente, las CRO se apresuraron a agregar capacidades virtuales y descentralizadas a sus ofertas de servicios. La tecnología de IA demostró ser invaluable en la creación y ejecución de dichos proyectos para ayudar a sintetizar datos y acelerar los procesos de ensayos clínicos.
Los gigantes tecnológicos persiguen el descubrimiento de fármacos y la biotecnología
Los éxitos mencionados anteriormente de DeepMind y Meta de Alphabet para resolver acertijos de investigación en biología básica, como predecir estructuras de proteínas a escala utilizando modelos de lenguaje y aprendizaje profundo, son solo la punta del iceberg: casi todos los gigantes tecnológicos líderes ahora están en el negocio de las ciencias de la vida. , de alguna manera.
Alphabet (una empresa matriz de Google) tiene docenas de inversiones en proyectos de ciencias de la vida, incluido el motor de búsqueda de reactivos basado en IA BenchSci, la IA y la física cuántica con sede en China en la empresa de descubrimiento de fármacos XtalPi, la empresa de genómica personal 23andMe y el desarrollo de fármacos impulsado por IA. unicornio OWKIN por nombrar algunos. En 2021, Alphabet, junto con DeepMind, lanzó Isomorphic Labs para centrarse en aplicar inteligencia artificial para descifrar la biología básica y el descubrimiento de fármacos.
Además de muchos otros proyectos y actividades en investigación farmacéutica y biotecnología, Alphabet tiene una entidad a gran escala, Verily, dedicada a las ciencias biológicas y la tecnología médica.
Microsoft, un desarrollador de software global, tiene una gran presencia en las ciencias de la vida, con docenas de colaboraciones de investigación con grandes farmacéuticas, proporcionando sus infraestructuras para manejar big data utilizando modelos de aprendizaje automático a gran escala. Entre las últimas iniciativas de Microsoft se encuentra modelo Moler, una nueva herramienta que está desarrollando el equipo de química generativa de la empresa en colaboración con Novartis. El modelo MoLeR, a diferencia de otras herramientas generativas, utiliza el aprendizaje profundo para generar nuevas estructuras basadas en un andamio determinado que actúa como base inicial para el proceso generativo. Otro ejemplo es AI4Ciencia, una nueva empresa de Microsoft que combina química computacional, física cuántica, aprendizaje automático, biología molecular, dinámica de fluidos e ingeniería de software para hacer realidad una visión del llamado "quinto paradigma" de la ciencia.
RELACIONADO: Cómo "Big Tech" está ganando lentamente los mercados farmacéuticos
Una empresa particularmente activa en este contexto es un productor de hardware para la industria del juego y las computadoras personales, NVIDIA. Esta empresa de tecnología ha lanzado Clara Discovery, que es una colección de marcos, aplicaciones y modelos de IA que permiten el descubrimiento de fármacos acelerado por GPU, con soporte para la investigación en genómica, proteómica, microscopía, detección virtual, química computacional, visualización, imágenes clínicas y procesamiento del lenguaje natural (PNL). Y en marzo de 2022, la compañía presentó Clara Holoscan MGX™, una plataforma para que la industria de dispositivos médicos desarrolle e implemente aplicaciones de IA en tiempo real en el perímetro, específicamente diseñadas para cumplir con los estándares regulatorios requeridos. Clara Holoscan tiene como objetivo una arquitectura de referencia de grado médico todo en uno, así como soporte de software a largo plazo, para acelerar la innovación en la industria de dispositivos médicos.
El futuro de la IA en el descubrimiento de fármacos: todo lo “cuántico”
La mayoría de las herramientas de software utilizadas para el descubrimiento de fármacos y la investigación biológica se basan en la mecánica molecular, una representación simplificada de las moléculas, que esencialmente las reduce a "bolas y palos": átomos y enlaces entre ellos. De esta manera, es más fácil de calcular, pero la precisión sufre mucho. Para obtener una precisión adecuada, se debe tener en cuenta el comportamiento electrónico de los átomos y las moléculas, es decir, considerar las partículas subatómicas: electrones y protones. De esto se tratan los métodos de mecánica cuántica (QM), y la teoría no es nueva, se remonta a las primeras décadas del siglo XX.
Sin embargo, los métodos cuánticos son excepcionalmente costosos desde el punto de vista computacional y, hasta décadas recientes, era una barrera prohibitiva para que la teoría cuántica influyera en el lado práctico de las cosas. Debido al crecimiento exponencial de la potencia informática disponible, los métodos cuánticos finalmente se están convirtiendo en herramientas valiosas en manos de los científicos.
Varias empresas están fusionando el aprendizaje automático y la teoría cuántica para mejorar sustancialmente las capacidades de modelado de sus sistemas de descubrimiento de fármacos. Por ejemplo, los científicos de XtalPi, una empresa de tecnología con sede en China y EE. UU. respaldada por Sequoia China, Tencent y Google, han creado su plataforma Intelligent Digital Drug Discovery and Development (ID4), que incorpora mecánica cuántica, inteligencia artificial y alto rendimiento. algoritmos de computación en la nube. ID4 permite predecir con alta precisión las propiedades fisicoquímicas y farmacéuticas de los candidatos a fármacos de molécula pequeña, así como sus estructuras cristalinas, elementos críticos en la I+D de fármacos.
Otra empresa que avanza en este campo es Aqemia, con sede en París. La empresa se centra en el diseño de novo basado en la estructura de moléculas similares al plomo mediante la combinación de inteligencia cuántica y artificial (IA). Un algoritmo mecánico estadístico único de inspiración cuántica que predice la afinidad entre un compuesto y un objetivo terapéutico con precisión y 10,000 XNUMX veces más rápido que la competencia. La IA de Aqemia puede generar compuestos con mayor precisión al recibir retroalimentación del predictor de afinidad.
Por último, está Pharmacelera, con sede en Barcelona, una empresa informática que aplica la teoría cuántica para impulsar el diseño de fármacos a través de sus dos paquetes de software principales: PharmScreen y PharmQSAR. La primera herramienta permite una detección virtual precisa basada en ligandos utilizando un algoritmo de alineación de ligandos 3D de alta precisión basado en los campos de interacción. Puede generar una mayor tasa de diversidad entre los clientes potenciales que los métodos y herramientas clásicos. El segundo, PharmQSAR, es una herramienta de relación estructura-actividad cuantitativa (QSAR) en 3D que permite una combinación de múltiples campos de interacción para realizar estudios CoMFA/CoMSIA.
RELACIONADO: 12 empresas que utilizan la teoría cuántica para acelerar el descubrimiento de fármacos
Otra tendencia tecnológica, más futurista, que explota la teoría cuántica, trata de crear una computadora cuántica. Con varias décadas de avances en la teoría cuántica y progreso simultáneo en varios campos de software y hardware, finalmente estamos entrando en la era de las computadoras cuánticas que se vuelven prácticamente viables.
Si bien estamos en los primeros días de la computación cuántica, varias empresas ya están integrando elementos de la computación cuántica en el descubrimiento de fármacos computacionales.
Por ejemplo, POLARISqb es un desarrollador con sede en el Reino Unido del primer software de descubrimiento de fármacos del mundo creado para computadoras cuánticas, que combina inteligencia artificial y un enfoque cuántico. En el corazón de la tecnología POLARISqb se encuentra la plataforma de diseño de fármacos Tachyon, que se utiliza para ejecutar trabajos de diseño molecular distribuido en la nube, administrado por un proceso automatizado que permite buscar grandes bibliotecas químicas mientras se ejecutan múltiples proyectos en paralelo. Al desarrollar software patentado para sistemas cuánticos, la compañía afirma que puede acelerar sustancialmente el diseño de fármacos y obtener pistas de mayor calidad. Debido al "agnosticismo" inherente del sistema Tachyon, puede funcionar en múltiples enfermedades e indicaciones.
Menten AI es una empresa emergente canadiense fundada en 2018 que desarrolla una plataforma de software para el diseño de proteínas impulsada por el aprendizaje automático y la computación cuántica. La compañía utiliza algoritmos de optimización cuántica patentados, que cree que pueden mejorar significativamente la precisión del descubrimiento de fármacos al tiempo que reducen el costo y el tiempo de desarrollo.
Para resumir este post, vamos a referirnos a una predicción del Dr. Christopher Savoie, Co-fundador y CEO de Zapata Computing, una empresa estadounidense de software cuántico, sobre investigaciones de punta en esta área, que expresó en una entrevista para BiopharmaTrend:
“Quantum será parte de todos, o casi todos, los flujos de trabajo de ciencia de datos y aprendizaje automático en biofarmacia en el futuro. Creo que será una parte integral de ella. Si puede obtener un modelo más preciso mediante el uso de tecnología cuántica, ¿por qué no lo haría, después de todo?
Los modelos de lenguaje grande avanzan a pasos agigantados en el descubrimiento de fármacos
Las empresas de biotecnología, como Medicina Insilico, inocenciay Exciencia, para ayudar al descubrimiento de fármacos.
ChatGPT ayuda a los científicos a interactuar con la IA y las herramientas de aprendizaje automático, lo que hace que los datos sean más accesibles. Por ejemplo, Insilico Medicine emplea ChatGPT para interactuar con su plataforma de descubrimiento de objetivos, PandaOmics, mientras que el fundador de Ainnocence Lurong P. prevé versiones especializadas como Bio ChatGPT o Med ChatGPT. Exscientia utiliza LLM para generar afirmaciones estructuradas y mecanicistas para sus gráficos de conocimiento.
Los LLM también sirven como motores de búsqueda avanzada en ciencias biológicas. Google y Mente profundaEl chatbot de Med-PaLM proporciona respuestas a preguntas médicas, mientras que BenevolenteAI parece entusiasmado con la función de complemento de recuperación de ChatGPT, que podría ayudar a personalizar la función de chat en función de sus propios datos.
A pesar del potencial de los LLM en el descubrimiento de fármacos, algunas empresas como Terapéutica BioXcel, Inc. y enteroma ser cauteloso acerca de la adopción de la tecnología, citando preocupaciones sobre la precisión y la privacidad.
Lo que está claro es que el surgimiento de ChatGPT y otros modelos generativos de IA, como AlphaFold de DeepMind, ha aumentado la conciencia de sus posibles aplicaciones en biotecnología, lo que alienta a las empresas a explorar sus beneficios en el descubrimiento y desarrollo de fármacos.
Temas: Tendencias industriales
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- PlatoData.Network Vertical Generativo Ai. Empodérate. Accede Aquí.
- PlatoAiStream. Inteligencia Web3. Conocimiento amplificado. Accede Aquí.
- PlatoESG. Automoción / vehículos eléctricos, Carbón, tecnología limpia, Energía, Ambiente, Solar, Gestión de residuos. Accede Aquí.
- Desplazamientos de bloque. Modernización de la propiedad de compensaciones ambientales. Accede Aquí.
- Fuente: https://www.biopharmatrend.com/post/615-pharmaceutical-artificial-intelligence-key-developments-in-2022/



