El FDA eSTAR incluye una lista de ocho opciones diferentes para un método de esterilización, pero ¿cómo selecciona el mejor método y lo valida?

¿Qué es el Día del Envase Estéril?
El Consejo de Fabricantes de Envases de Esterilización (SPMC) fundó Día del embalaje estéril en 2021 para reconocer y agradecer a todas las empresas de la cadena de suministro que trabajan juntas para ofrecer dispositivos innovadores, seguros y esterilizados para brindar excelencia en la atención al paciente. El Día del Empaque Estéril es el 8 de febrero de 2023, y el tema de la celebración de este año es "Diseñado para Proteger". SPMC ofrece cuatro consejos para celebrar el Día del Envase Estéril:
- Donar sangre (use este enlace para una cita) el 8 de febrero de 2023, a las MD&M Oeste en Anaheim
- Reconocer y agradecer a un estimado profesional de embalaje con quien colaboras para el éxito
- Apoye a la próxima generación de ingenieros de empaque (Desafío de diseño para estudiantes de FPA)
- Cuéntanos en una palabra qué significa para usted “Diseñado para proteger” (Rob eligió “Salvavidas”)
¡Gracias a Jan Gates!
[Contenido incrustado]
Cómo seleccionar el mejor método de esterilización
Varios factores determinan el mejor método de esterilización a utilizar para su dispositivo. El primer factor es si su dispositivo se entregará estéril o si el usuario final esterilizará el dispositivo. Si el usuario final es el responsable de esterilizar el dispositivo, los métodos más comunes utilizados por los hospitales son:
- esterilización por vapor
- esterilización con peróxido de hidrógeno
- Esterilización EO
La popularidad del tercer método está disminuyendo debido a las restricciones ambientales sobre las emisiones peligrosas del proceso de esterilización con óxido de etileno. El peróxido de hidrógeno está ganando popularidad porque puede usarse para materiales sensibles al calor, y el vapor de peróxido de hidrógeno reacciona con la humedad para formar una solución acuosa inofensiva. El vapor es el método de esterilización más común utilizado por médicos, dentistas y hospitales porque los esterilizadores de vapor son relativamente económicos y no se requieren productos químicos peligrosos.
El segundo factor a considerar al seleccionar un método de esterilización es si hay componentes sensibles al calor. Los plásticos se derretirán y degradarán en los ciclos de esterilización por calor seco, y algunos plásticos no pueden soportar la temperatura de un esterilizador de vapor. Por lo tanto, si su dispositivo está fabricado con plástico para reducir costos, peso, compatibilidad con resonancia magnética (MR) u otras razones, es posible que deba usar un método de esterilización con un proceso de temperatura más baja.
El tercer factor a considerar al seleccionar un método de esterilización es si los tubos largos y angostos requieren esterilización. Estas características de diseño son difíciles de esterilizar para cualquier proceso de esterilización basado en vapor, como vapor, peróxido de hidrógeno u óxido de etileno. Existen algunas estrategias de control de procesos que se pueden utilizar para esterilizar con gas:
- uso de un vacío extremo para mejorar la penetración del gas esterilizante
- asegurarse de que el dispositivo y los materiales de embalaje estén secos
- uso de ciclos más largos con más gas esterilizante
- uso de indicadores biológicos internos en el lugar de esterilización más difícil
El cuarto factor a considerar al seleccionar un método de esterilización es si el dispositivo incluye un líquido. Un líquido no se puede esterilizar con peróxido de hidrógeno, óxido de etileno o calor seco. En algunos casos, el líquido puede ser un esterilizante (es decir, ISO 14160:2021 para agentes esterilizantes químicos líquidos). Hay tres soluciones populares para la esterilización de un dispositivo que incluye líquido:
- esterilización por vapor, suponiendo que el líquido no contenga componentes sensibles al calor (p. ej., proteínas)
- esterilización por filtración, generalmente combinada con llenado aséptico y recipientes preesterilizados)
- esterilización por radiación con eBeam o Gamma
eBeam y Gamma también se utilizan para esterilizar productos en los que se desea la reticulación del polietileno de ultra alto peso molecular (UHMWPE) o cuando es imposible que un gas esterilizante penetre en todas las áreas de un dispositivo.
¿Cuáles son los estándares de validación de esterilización aplicables para cada método de esterilización?
Como se muestra en la captura de pantalla eSTAR de FDA anterior, se pueden seleccionar ocho posibles métodos de esterilización para esterilizar un dispositivo médico en una presentación 510k o De Novo. Cada método de esterilización tiene un estándar aplicable diferente que debe usarse para validar el proceso de esterilización, pero en todos los casos, el proceso de esterilización debe dar como resultado un nivel de garantía de esterilidad (SAL) de 10-6.
La FDA considera que los métodos de esterilización Establecidos A (Est A) tienen una larga historia de uso seguro y eficaz, mientras que la FDA no ha reconocido un estándar de consenso dedicado para los métodos de esterilización Establecidos B (Est B). Sin embargo, hay ejemplos de dispositivos que han recibido la aprobación FDA 510k utilizando cada uno de los métodos de esterilización no tradicionales (es decir, métodos Est B). Los fabricantes generalmente adaptarán los estándares internacionales existentes para la validación de la esterilización para validar los métodos no tradicionales. Hay información publicada sobre el desarrollo, validación y control de rutina para estos procesos de esterilización no tradicionales.
Los enlaces a cada uno de los estándares reconocidos se proporcionan a continuación:
- Vapor (Calor húmedo) (Est A) – ISO 17665-1:2006, Esterilización de productos para el cuidado de la salud. Calor húmedo. Parte 1: Requisitos para el desarrollo, validación y control de rutina de un proceso de esterilización para dispositivos médicos.
- Óxido de etileno (EO, EtO) (Est A) – ISO 11135:2014, Esterilización de productos para el cuidado de la salud – Óxido de etileno – Requisitos para el desarrollo, validación y control de rutina de un proceso de esterilización para dispositivos médicos; e ISO 10993-7:2008, Evaluación biológica de dispositivos médicos - Parte 7: Residuos de esterilización con óxido de etileno
- Radiación (Est A) – ISO 11137-1:2006, Esterilización de productos para el cuidado de la salud – Radiación – Parte 1: Requisitos para el desarrollo, validación y control de rutina de un proceso de esterilización para dispositivos médicos; ISO 11137-2:2013, Esterilización de productos para el cuidado de la salud. Radiación. Parte 2: Establecimiento de la dosis de esterilización.
- Calor seco (Est A) – ISO 20857:2010, Esterilización de productos para el cuidado de la salud – Calor seco – Requisitos para el desarrollo, validación y control de rutina de un proceso de esterilización para dispositivos médicos
- Peróxido de hidrógeno (Est B): ISO 22441:2022, Esterilización de productos para el cuidado de la salud. Peróxido de hidrógeno vaporizado a baja temperatura. Requisitos para el desarrollo, validación y control de rutina de un proceso de esterilización para dispositivos médicos (esta norma no está reconocida por la FDA de EE. UU. )
- Ozono (Est B): este es un nuevo método que utiliza gas ozono, y el método de acción es similar al EO y H2O2
- Sistemas de bolsas flexibles (Est B): la norma ISO 22441:2022 debe usarse para la validación de sistemas de bolsas flexibles con peróxido de hidrógeno, pero en lugar de validar el proceso con tres medios ciclos que son la mitad de la duración del ciclo completo, en su lugar, debe use tres medios ciclos que usen la mitad del volumen de esterilizante de un ciclo completo; este método es utilizado por andersen científico para sus esterilizadores de bolsas EO.
- Métodos novedosos: ISO 14937:2009, Esterilización de productos para el cuidado de la salud. Requisitos generales para la caracterización de un agente esterilizante y el desarrollo, validación y control de rutina de un proceso de esterilización para dispositivos médicos.
¿Cuándo se debe utilizar un método de esterilización novedoso?
Los métodos de esterilización novedosos solo deben usarse cuando ninguno de los métodos de esterilización tradicionales (Est A) y no tradicionales (Est B) no funcionen. Por ejemplo, el llenado aséptico combinado con la filtración de líquidos es una estrategia común para las jeringas precargadas si el líquido es sensible a la esterilización por radiación. La esterilización con ácido peracético se ha utilizado durante mucho tiempo, pero el método de esterilización no ha ganado una gran popularidad. El ácido peracético también se puede combinar con peróxido de hidrógeno. También existe un estándar de validación de formaldehído y vapor a baja temperatura (es decir, ISO 25424:2019). La esterilización con luz ultravioleta es un proceso que a veces se usa cuando los materiales son sensibles a las altas temperaturas y donde la luz ultravioleta puede penetrar todas las superficies. El dióxido de nitrógeno se desarrolló como un esterilizante más ecológico similar al óxido de etileno. X-Ray es un nuevo tipo de esterilización por radiación que se está desarrollando como una alternativa de alta velocidad a Gamma y eBeam, pero la esterilización por rayos X también tiene la ventaja de poder controlar un rango de dosis más estrecho que los procesos Gamma y eBeam.
Estándares de consenso para la validación de la esterilización
También hay estándares de apoyo adicionales que necesitará para la validación de su proceso de esterilización. La siguiente es una lista parcial de los estándares que podría considerar:
- ISO 11737-1:2018, Prueba de biocarga para bacterias y hongos aerobios
- Prueba de eficacia antimicrobiana USP<51>
- Candida albicans (una levadura... las levaduras son una forma de hongo)
- Aspergillus brasiliensis (un moho filamentoso…también un hongo)
- Escherichia coli (una bacteria… más conocida como “E. coli")
- Pseudomonas aeruginosa (una bacteria… muy problemática industrialmente)
- Staphylococcus aureus (una bacteria… mejor conocida como “Staph”
- USP<61> Prueba de carga biológica o límites microbianos (Recuento total de microbios aeróbicos = TAMC; Recuento total de levaduras y mohos = TYMC)
- USP<62> Pruebas de organismos o patógenos objetables
- USP<63> Pruebas de micoplasma
- USP<71> Bacteriostasis/Fungistasis (es decir, B/F) Pruebas de esterilidad
- ISO 11138-1:2017, Esterilización de productos para el cuidado de la salud. Indicadores biológicos. Parte 1: Requisitos generales.
- ISO 111140-5:2017, Esterilización de productos para el cuidado de la salud. Indicadores químicos. Parte 5: Indicadores de clase 2 para hojas y paquetes de prueba de eliminación de aire de Bowie y Dick.
- ISO 17664-1:2021, Procesamiento de productos para el cuidado de la salud. Información que debe proporcionar el fabricante de dispositivos médicos para el procesamiento de dispositivos médicos. Parte 1: Dispositivos médicos críticos y semicríticos.
Pruebas de envejecimiento y vida útil
El estándar actual para los estudios de envejecimiento acelerado es ASTM F1980: 2021 “Guía estándar para el envejecimiento acelerado de los sistemas de barrera estériles y Dispositivos médicos se revisó y lanzó recientemente para incluir dispositivos médicos”. Jan Gates explica que el "y" solía decir "por". El lenguaje se actualizó con más información sobre los efectos de la humedad del producto para acompañar el título. Jan tuvo la amabilidad de escribir un Protocolo de prueba de vida útil para nosotros basado en esta nueva versión del estándar. El protocolo incluye requisitos para pruebas de edad aceleradas y en tiempo real de un producto. Si necesita capacitación básica sobre cómo validar la vida útil de su dispositivo, tenemos un seminario web en venta sobre la esterilidad y la vida útil. También grabamos un seminario web actualizado el 19 de enero de 2023, como parte de las actualizaciones eSTAR de la FDA para nuestro Curso 510(k).
Pruebas de acondicionamiento de distribución y pruebas de rendimiento de empaque
También existen estándares para pruebas de acondicionamiento de distribución (es decir, ASTM D4169-22). Jan Gates tuvo la amabilidad de escribir un artículo de 20 páginas Protocolo de calificación de envío de acondicionamiento de distribución para Medical Device Academy basado en el estándar ASTM. El protocolo está disponible para su compra en el enlace de arriba. Jan también escribió un artículo de 18 páginas Protocolo de prueba de rendimiento de embalaje para nuestros clientes de acuerdo con ISO-11607 1 y ISO-11607 2.
¿Dónde puede encontrar un procedimiento para cada método de esterilización?
ISO 13485:2016, Cláusula 7.5.7 es específica para los "Requisitos particulares para la validación de procesos para esterilización y sistemas de barrera estéril". Esta cláusula incluye el requisito de establecer procedimientos para la validación de la esterilización y la validación de sus sistemas de barrera estéril. Incluso si su empresa usa un protocolo y procedimientos establecidos por un fabricante contratado, aún necesita establecer uno o más procedimientos internos para cumplir con este requisito si tiene productos estériles. La siguiente es una lista de procedimientos vendidos por Medical Device Academy:
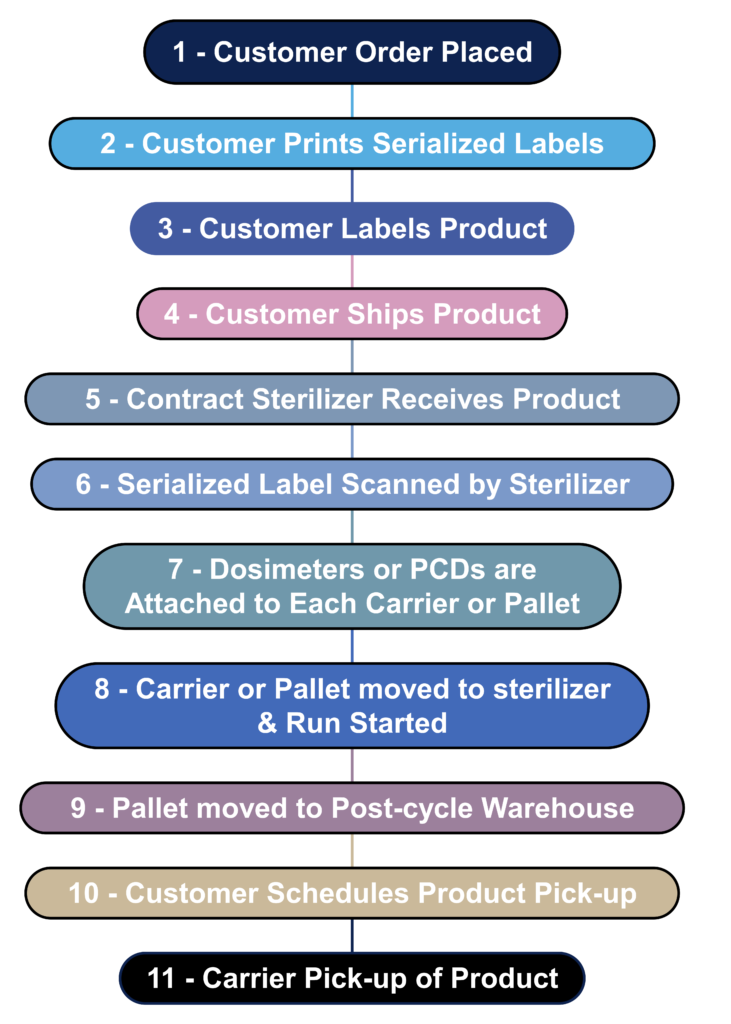
¿Cuál es el flujo del proceso para la esterilización por contrato?
La mayoría de los fabricantes de dispositivos no esterilizan sus dispositivos internamente. En cambio, la esterilización se subcontrata a un esterilizador contratado. El siguiente diagrama de flujo de proceso es un diagrama de flujo de proceso hipotético para un proceso de esterilización por contrato. El único paso que no se incluye en este flujo de proceso es la incubación de indicadores biológicos porque los procesos de esterilización gamma y eBeam utilizan dosímetros en lugar de indicadores biológicos. La naturaleza de los indicadores biológicos también está cambiando rápidamente porque los fabricantes están desarrollando indicadores biológicos de "prueba rápida". En 2008 trabajé extensamente con indicadores biológicos autónomos que eliminaron la necesidad de utilizar una técnica aséptica para transferir indicadores biológicos a medios de cultivo. Además, completo un estudio de reducción de la incubación para validar un ciclo de incubación más corto de 48 horas en lugar de la típica prueba de esterilidad de 7 días. Terragene es uno de los fabricantes que desarrolla tecnología de próxima generación para indicadores biológicos que permite leer los resultados en segundos en lugar de 48 horas. Esta tecnología de última generación también incorpora lectores de códigos de barras y lectores en red para garantizar la trazabilidad de cada indicador biológico y lector.
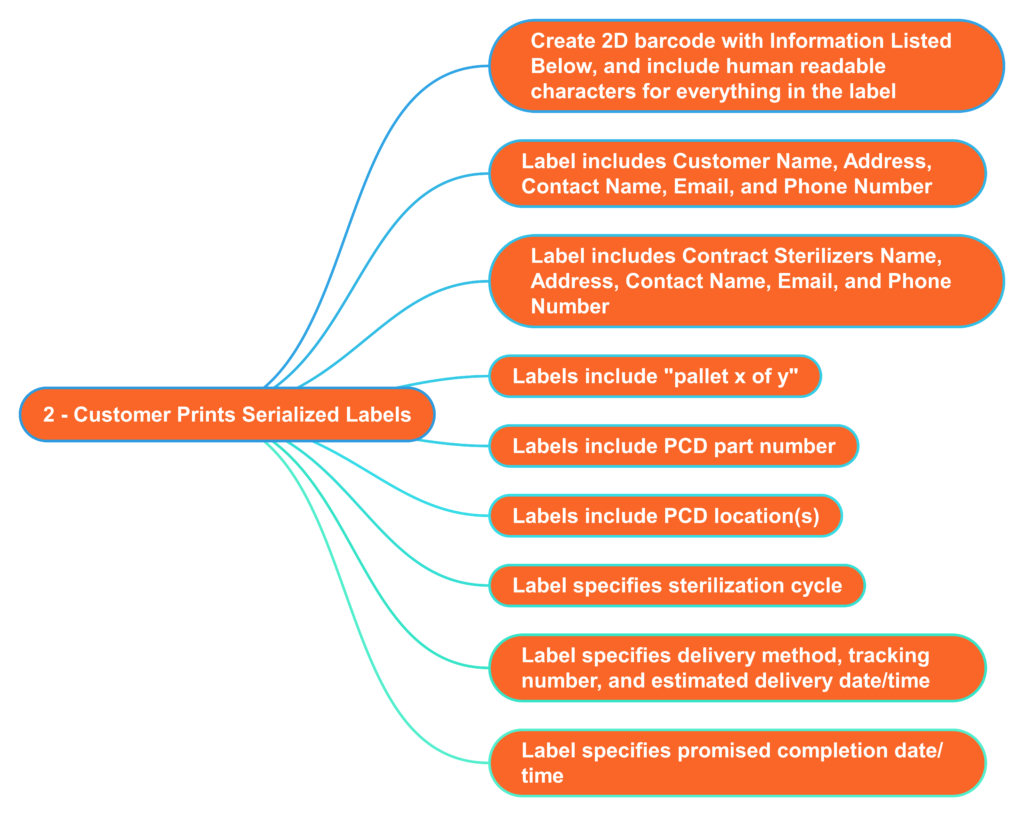
¿Qué información deben incluir las etiquetas serializadas para los esterilizadores por contrato?
En los "viejos tiempos" (c. 2005), solía imprimir etiquetas para cada palé que enviábamos a las instalaciones de Isomedix en Northboro, MA. La etiqueta identificaba de quién era el producto y qué queríamos que hiciera Isomedix con el producto (p. ej., esterilización gamma a 25-40 kGy). En ese momento, recién comenzábamos a incorporar códigos de barras en el etiquetado bajo demanda para facilitar la trazabilidad. 18 años después, las empresas siguen estancando la implementación de etiquetas con códigos de barras bajo demanda. Casi todos los muelles de envío tienen un lector de código de barras y la tecnología es económica. Por lo tanto, debe considerar crear una plantilla para etiquetas con código de barras bajo demanda con toda la información que se detalla a continuación. Esto reducirá el riesgo de errores por parte del esterilizador contratado y le permitirá identificar rápidamente cuándo se cometió un error. Los esterilizadores contratados también deben exigir esta información en el etiquetado del producto como un control de riesgo adicional. Todos los indicadores biológicos y dosímetros están etiquetados con Códigos de barras UDI ahora. Por lo tanto, los esterilizadores contratados deberían poder crear controles de procesos sólidos que garanticen la trazabilidad entre los códigos de barras de su producto etiquetado con los códigos de barras del indicador biológico o dosímetro.
Publicado en: Validación de esterilización, Validación
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- Platoblockchain. Inteligencia del Metaverso Web3. Conocimiento amplificado. Accede Aquí.
- Fuente: https://medicaldeviceacademy.com/sterilization-method/



